- Gösterim: 143944
Cilt, yaklaşık 2 m²'lik yüzey alanı ile vücudumuzun en büyük organıdır. Mikroorganizmalar, kimyasallar, toksinler, UV ve radyasyon gibi çevresel etkilere karşı en dış bariyeri oluştururken, çevre ile vücut arasındaki hemostazı sağlamaktadır. Cildin bütünlüğünün bozulup hasarlanması, mikroorganizmalar, sıcak-soğuk, güneş, kesici-batıcı bir cisim veya kimyasal bir madde gibi herhangi bir dış etkenle olabileceği gibi, vücut-deri hastalıklarına bağlı olarak içsel nedenlerle de gelişebilmektedir. Cildin hasarlanması ile kusursuz çalışan bir mekanizma devreye girmekte; bu mekanizma fizyolojik yara iyileşmesidir. Fizyolojik yara iyileşmesi, doku bütünlüğü ve fonksiyonunu tekrar sağlayan hücresel ve biyokimyasal mekanizmalardan oluşmaktadır. Yara iyileşme bozuklukları, patolojik yara iyileşmesi olarak tanımlanır. Patolojik yara iyileşmesi, sıklıkla farklı klinik özelliklere sahip olan skar ve nedbe izi gelişimi ile sonlanmaktadır. Tanım olarak, yara izleri (Latince: cicatrix) ciltte dermisin derin katmanlarını içeren patolojik yara iyileşmeleridir. Cilt seviyesinin altına çökmüş lezyonlar atrofik yara izleri olarak görülebildiği gibi, deriden kabarık hipertrofik yara izleri ve keloidler gibi aşırı doku büyümesi ile karakterize olabilmektedir. Kozmetik sorunlara ek olarak, genellikle fonksiyonel bozukluklara da neden olabilmektedir. Patolojik yara iyileşmesi, ekzojen ve endojen faktörlerden etkilenebilir; lokal nedenlere (enfeksiyon ve kan dolaşımı) ek olarak, sistemik faktörler de önemli bir rol oynamaktadır (sistemik inflamasyon, metabolik, endokrin ve onkolojik hastalıklar). Patolojik yara iyileşmesinde sigara kullanımı ve beslenme gibi bireysel yaşam tarzı alışkanlıkları da önemlidir. Patolojik yara iyileşmesi ve skarlar, dünya çapında sağlık sistemleri üzerinde önemli bir etkiye sahiptir.
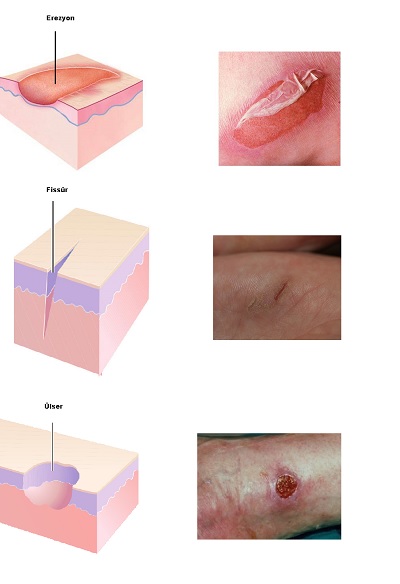
Ciltte yaralanma, doku hasar derinliğine göre erozyon, ülser ve fissür olarak tanımlanır. Erozyon, deride yüzeysel doku kayıplarını tanımlarken, fissür ya da çatlak, deride dikey yaralanma ile doku kayıplarını tanımlamaktadır. Ülserler ise cilt yüzeyinden dermise kadar olan derin doku kayıplarını tanımlamaktadır.
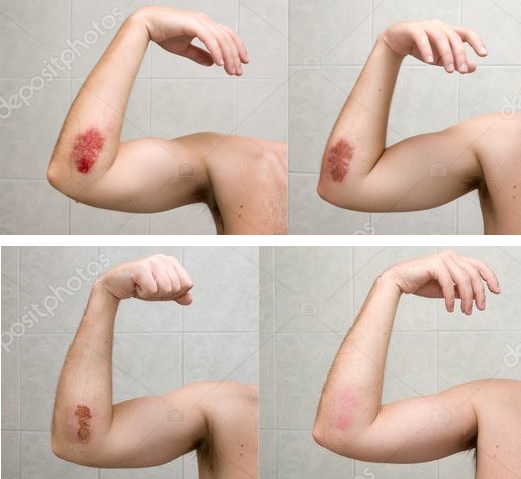
Cilt dokusunun bütünlüğünün kaybı, yara dokusunun oluşumu fizyolojik yara iyileşme süreçlerinin başlamasına yol açar. Cilt yaralarının iyileşmesi için kesin bir süre verilemez. Bu süre kişinin genel sağlık durumuna, kan dolaşımına, yaranın oluşma nedenine, vücutta yerleşim yeri ve yaranın türüne, yarada enfeksiyon olup olmamasına... gibi değişken birçok faktöre bağlıdır. Yani her yara kendi özelliklerine göre iyileşir. Ancak 3 aydan daha uzun süren yaralar kronik yara olarak tanımlanmaktadır. Yara iyileşmesi doku bütünlüğünü yeniden sağlamayı amaçlar. Ancak bazı durumlarda, patolojik yara iyileşmesinde doku bütünlüğü tam olarak sağlanamaz. Doku iyileşmesi uzayabileceği gibi sonrasında skar-nedbe-iz gelişebilir ve fibrozis(normal dokunun yerini destek dokusunun alması) oluşumuyla sonlanır.
Fizyolojik Yara İyileşmesi
Yara iyileşmesi, dokuda hücreler ve aracıların karmaşık bir etkileşimi ile ardışık ve örtüşen bölümlerden oluşmaktadır. Yara iyileşmesi sadece yara bölgesiyle sınırlı değildir; tüm vücudu kapsayan hücresel, fizyolojik ve biyokimyasal olaylar bütünüdür. Başarılı bir fizyolojik yara iyileşmesi, yara bölgesinde inflamasyon yapıcılar ile inflamasyon önleyiciler ve doku yıkıcılar ile doku onarıcılar arasındaki dengedir.
Yara iyileşmesi temel olarak ardışık ve örtüşen üç aşamada gerçekleşir.
1. Hemostaz ve inflamasyon safhası(1-5 gün sürmekte)
2. Proliferasyon-Hücresel Çoğalma Safhası( 5-14. günler)
3. Maturasyon-Doku Olgunlaşması Safhası (14. günden sonrası)
İnflamasyon, hemostaz safhası
İnflamatuar faz, yara iyileşmesinin başlangıcını işaret eder. Cilt hasarının olduğu alandaki yerleşik hücrelerin aktivasyonu ve kan dolaşımındaki hücrelerin yaraya alınması ile karakterize edilir. Yara dokusunda inflamatuvar reaksiyon hemostazdan önce gerçekleşir. Dokuda kanama ve damarsal bütünlüğün korunması hemostaz ile sağlanır. Hasarlı doku damarlarında salınan subendotelyal kollajen, pıhtılaşma sürecinin içsel ve dışsal yollarını aktive eder. Yaralanmayı takiben yara bölgesindeki yıkıma uğramış damarlar hemen daralır. Damar duvarı zedelendiğinde trombositler( kan hücrelerinden kanama ve doku onarımında görevli ) açılan damar duvarındaki kollajenle temas ederek aktive olurlar. Böylece hem damar duvarına hem de birbirlerine yapışırlar. Trombositlerden hasarlı dokuya doku ürünler salınır. Bunlardan Tromboksan A2’nin aktivasyonu ile trombositler geçici ilk pıhtı tıkacı oluşturarak başlangıçta kanamayı azaltırlar. Daha sonra bu tıkaç içerisinde fibrin oluşumu ile kalıcı pıhtı oluşmaktadır. Hemostazisi düzenlemek için fibrin pıhtısı nötrofiller ve monositler için iskelet görevi yapar. Daha sonraki aşamada trombositlerden salınan serotonin ve diğer damar daralma-vazokonstriktör ajanlarla vazokonstriksiyon gelişerek kanama azalır. Başlangıçta gelişen damarlarda daralma prostaglandin ve kompleman sisteminin aktivasyonu ile yerini yaygın damarlarda genişleme-vazodilatasyona bırakır. Genişlemiş damarlar doku hasarlı alana kan hücrelerinin geçişini arttırmakta ve hücreler arasında inflamatuar eksuda toplamakta. Kollajen, trombosit, trombin ve fibronektin ile birlikte diğer hücresel bileşenlerden oluşan bir pıhtı, sitokinler ve büyüme faktörleri tarafından çeşitli hücrelerin (nötrofiller, monositler, fibroblastlar ve endotel hücreleri) alana gelerek yerleştiği geçici bir matris oluşturur. Aynı zamanda, kompleman sistemi ve bağışıklık sistemi aktive edilir. Doku zedelenmesi dokuda birçok kimyasal mediatör ve hücreler arası bilgi aktarımını sağlayan sitokinlerin salınımına neden olur. Bu maddeler yara dokusu ve çevresinde aktivasyon ve inhibisyon yaparak birçok kompleks olayı başlatır.
İnflamatuar faz, yara iyileşmesinin başlangıcını işaret eder ve birincil hemostaz, yerleşik hücrelerin aktivasyonu ile dolaşan hücrelerin yaraya alınmasıyla karakterizedir.
Bağışıklık sisteminin bir parçası olan nötrofiller, erken inflamatuar fazın başlıca aktörleridir. Hasarlı dokuda ortaya çıkan interlökin (IL)-1, tümör nekroz faktörü (TNF)-α, dönüştürücü büyüme faktörü (TGF)-β, trombosit faktör 4 ve var ise bakteriyel bileşenler, nötrofilleri dolaşım sisteminden hasarlı dokuya çekmektedir. Eş zamanlı olarak, hücre yüzey deseni tanıma reseptörleri (PRR'ler), istilacı mikroorganizmalar (patojenle ilişkili moleküler desenler, PAMP'ler) ve hasarlı dokudan (hasarla ilişkili moleküler desenler, DAMP'ler) gelen ekdış tehlike sinyallerini tanır. Bunu inflammasom ve kaspaz aktivasyonu ile inflamatuar sitokinlerin (IL-1 dahil) salınmasıyla bir sinyal yolunun tetiklenmesi izler. Salınan mediatörler vazodilatasyona yol açar ve nötrofiller başta olmak üzere kan hücrelerinin yara bölgesine göçünü artırır.
Daha sonra yara alanına monosit isimli kan hücreleri hakim olmaya başlar. Yaralanmadan 72 saat sonra hakim olan hücreler makrofajlardır. Dolaşımdaki monositler dokuya geçtiklerinde makrofajlara farklılaşır, yerleşik hale gelirler ve diğer hücrelerin işlevini düzenlerler (fibroblastların uyarılması, keratinositlerin aktivasyonu), anjiyogenezi desteklerler ve yara debridmanına katkıda bulunurlar. Makrofajlar, diğer faktörlerin yanı sıra TGF-β tarafından aktive edilir ve yara iyileşmesinin farklı zaman noktalarında farklı sitokin salınımları ile farklı işlevsel programlar üstlenirler. Erken makrofaj popülasyonları (M1 alt kümesi) inflamatuar özelliklere sahipken, yara iyileşmesinin sonraki aşamalarındaki makrofajlar fibroblast farklılaşmasını destekler (M2 alt kümesi). Bu denge, başarılı ve fizyolojik yara iyileşmesi için çok önemlidir ve patolojik yara iyileşmesinde başlangıç noktası olabilir.
İnflamasyonun yara iyileşmesinde bazı tartışmalar var. Anne rahminde bebekte-fetuste yaralanmalar sonrası inflamasyon fazı erişkine göre daha kısadır ve yara iyileşirken skatris gelişmememekte. İnflamasyon yara iyileşmesinde ik aşama ancak kısa süreliolması skatris gelişimini önleyebilir. Son zamanlardaki dokuda bir sitokin olan aktive protein C (APC) nin yarada inflamasyon sürecini baskıladığı, anjiogenezi stimüle ettiği ve dermisin yeniden büyümesi ve epidermal rejenerasyonu sağlayarak yara iyileşmesini hızlandırıdığı gösterilmiştir.
Proliferasyon-Hücresel Çoğalma Fazı
İnflamatuar fazdan proliferatif faza geçiş, yara iyileşmesinde kritik bir adımdır. Bu fazda, odak noktası epitelizasyon, anjiyogenez ve granülasyon dokusu oluşumu ile yara bölgesinin yeniden organizasyonudur. Cilt doku hasarında bazal membran değişiklikleri olmuş ise epidermal rejenerasyon dermiste bulunan deri eklerinden (çoğunlukla kıl folikülleri) ve yara kenarlarından gelen kök hücreler tarafından gerçekleştirilir. Aynı zamanda, kılcal damarlar yara yatağına doğru büyür ve besin ile oksijen sağlayarak iyileşme sürecinin temelini oluşturur (anjiyogenez). hasar sırasında bazal membran sağlam ise birkaç gün içinde bazal kök hücrelerden keratinositlerin artan büyümesi, tam epidermal rejenerasyonla birlikte gerçekleşir. Hücresel düzeyde, epidermal farklılaşmayı kontrol eden keratinositlerin kalsiyum duyarlılığında değişiklikler vardır. Makrofajların ve fibroblastların ilerleyici göçüyle, geçici pıhtı matrisi granülasyon dokusuna dönüşür. Fibroblastlar kollajen üretir ve kasılma yoluyla yara kenarlarını uyarlayan α-düz kas aktini (SMA) üreten miyofibroblastlara dönüşür. Başlangıçta, bağ dokusu matrisi olgunlaşmamış kollajen liflerinden (tip III) ve glukozaminler ile fibronektinden oluşur. Proliferasyon fazı, fibroblast ve makrofajların göçüyle yönlendirilen granülasyon dokusunun oluşumuyla yara bölgesinin organizasyonu ile karakterizedir. Bu aşamanın başlaması için iyi bir oksijenasyon ve beslenme şarttır. Bu aşamada vitamin C, prolinin hidroksiproline dönüşümü için şarttır.
Yaralanmadan sonraki iyileşmenin ikinci evresi, yaklaşık 4. günde başlamakta ve 12 güne kadar sürmekte. Bu dönemde hasarlanan ve yitirilen dokuların yeniden yapılmakta-doku devamlılığı sağlanmakta. Bu dönemde yara alanına fibroblastlar ve endotel hücreleri göç etmekte. sonra, geçici hücre dışı destek dokusu oluşmaya başlar. Derinin kalıcı elamanları fibroblastlar tarafından üretilmeye başlanmaktadır. Fibroblastlar yara iyileşmesinde görev alan en önemli mezankimal hücrelerdir. Hem “üretim” hem de “mekanik” görevleri vardır. Fibroblastlar kollagen liflerini üretirler. Kollagen de yaranın kontraksiyonunu ve gerilme kuvvetini oluşturur. Bu safhada epitelizasyon ve kontraksiyon gelişir. Yara kontraksiyonu ile yara büyüklüğü azalır. Bu olay çoğunlukla miyofibroblastlarca gerçekleşir. Granülasyon dokusu oluşup epitelizasyon tamamlanınca proliferasyon aşaması sona erer.
Endotel hücreleri bu evrenin diğer önemli parçası olan anjiogenezde görev alırlar. Endotel hücreleri yaraya yakın sağlam venüllerden göç ederler. Bu migrasyon, replikasyon ve ve yeni kapiller tübül formasyonu TNF alfa, TGF- beta ve VEGF gibi sitokinlerin ve büyüme faktörlerinin etkisi altındadır. VEGF özellikle makrofaj kaynaklıdır ve reseptörleri endotel hücrelerinde bulunur.
Doku Olgunlaşması - Matürasyon (Remodeling) Fazı
İnflamasyon ve proliferasyon evresinden sonra yarada yavaş yavaş bu faz başlar ve yara iyileşmesi ile stabilitesi için kritik öneme sahiptir. Yara iyileşmesinin en uzun süren aşamasıdır. Yara iyileşmesinin her aşamasında olduğu gibi, bu aşama da diğerleriyle üst üste binmiştir. İnsanlarda yara matürasyonu, klinik olarak, yara kontraksiyonu – alanın büzülerek daralması, kızarıklık ve yara kalınlığında azalma, yara kuvvetinde artma ile karakterizedir. Matürasyon fazında yara kalınlığı azalırken, yaranın gerilmeye dayanım kuvveti ters orantılı olarak artar.
Kollajen üretimi; yaralanmadan sonra ortalama 21. güne kadar sürekli bir artış gösterir. Bu aşamadan sonra kollajen sentezinde bir azalma gözlenir.Yara iyileşmesinin 21. gününde maksimum kollajen miktarına ulaşılsa da, yaranın tensil kuvveti normalin ancak % 20’si kadardır. 6. haftada yaranın tensil kuvveti, olması gerekenin % 80’ine ulaşır. 21. günle 6. hafta arasında geçen ve yara kuvvetinin arttığı bu dönemde gerçekleşen asıl olay, kollajen yıkımı ve yeniden düzenlenmesidir. Yara iyileşmesinin erken dönemlerine kollajen fibrilleri düzensiz şekilde dizilmişlerdir. Bu, iyileşmenin erken döneminde, yüksek kollajen miktarına rağmen, yara kuvvetindeki zayıflığı açıklar. Birkaç aydan birkaç yıla kadar süren bir süre boyunca tip III kolajen, tip I kolajen liflerinin kalın demetleriyle değiştirilir.
Bu dönemde kolejen dışında glikozaminoglikanlarda yapılmakta. Yarada bulunan ana glikozaminoglikanlar dermatan ve kondroitin sülfattır. Fibroblastlar yara iyileşmesinin ilk 3 haftası konsantrasyonları arttırarak bu bileşenleri sentez ederler. Fibrillere ve fiberlere kollajen subünitlerinin bağlanmasının sülfatlanmış proteoglikanlarca üretilen kafeslere bağımlı olduğu öne sürülmektedir. Sülfalanma derecesinin kollajen fibrillerinin konfigürasyonunun belirlenmesinde kritik öneme sahip olduğu izlenmektedir. Yara iyileşmesinin ileri zamanlarında proteoglikan içeriği kademeli olarak azalır.
Bu evrede remodelling başlar, bu da kollajenin ve glikozaminoglikanların reorganizasyonu ile ilişkilidir. Kollajen matriks MMP ler tarafından yıkılır, son yara yeri kollajeni kollajenolizis ve kollajen yapımı arasındaki denge sonucu şekillenir. MMP ler kollajen yanısıra elastin, laminin, fibronektinin hidrolizini katalize eder ve sitokin ve büyüme faktörlerini de işler. Normal ve bütünlüğü korunmuş deride MMP ler çok düşük miktarlardadır. MMP-7 ve MMP-19 sadece ter ve yağ bezlerinde sürekli olarak üretilir. Kollajen sentezi ve yıkımı sitokinler ve büyüme faktörleri tarafından denge halinde tutulur. TGF beta gibi bazı sitokinler hem yapım hem yıkımda görev alabilirler. Gap junction protein connexin 43 (Cx43) yara iyileşmesi, re-epitelizasyon, ekstraselüler matriks oluşumuna rolü vardır. Cx43’ün mekanizması tam olarak bilinmese de özellikle TGF-beta sinyalizasyonunu ve fibrozisi düzenlediği hafif dereceli sikatris formasyonuna yol açtığı bilinmektedir.
Granülasyon dokusu stabil skar dokusuna dönüşür. Bu süreçte yerleşik hücreler programlanmış hücre ölümüne (apoptozis) uğrar. Hücre rejenerasyonu ve yıkımı(degradasyonu) arasındaki denge bozulduğunda aşırı doku üretimi meydana gelir(fazla gelişen skar dokusu, hipertroifk skar gibi).
Skar matürasyonuyla beraber, klinik olarak gözlemlenen kızarıklık azalışı yara içindeki yeni damarlanma yoğunluğunun değiştiğini gösterir. Matür skar, granülasyon dokusuna oranla daha az damarlanma içermektedir.
Yara iyileşmesi, dokunun yeniden yapılandırılması dermoepidermal yapısal birimin orijinal şekline ve stabilitesine sahip olmadığı, karakteristik bir kolajenöz bağ dokusu bileşimine sahip bir normal skar oluşumuyla sonuçlanır.
Deri iyileşmesinde en önemli süreç aslında deri epitel hücrelerinin epitelyal mezenkimal dokuya geçişdir. Deride epitel ve mezenkimal hücrelerden ibarettir. Deri eitel hücreleri meznkimaldokuya geçerek fibroblast, kan damarlarının düz kas hücreleri, perisitler gibi mezenkimal hücrelere farklılaşırlar. Bu farklılaşmada deri epitel hücrelerinde moleküler değişiklikler ile mezenkimal fenotip gelişir. Bu değişim bu hücrelere mezenkimal dokuya göç etme kapasitesi, apopitoza direnç ve mezenkimal hücreler arası matriksin üretim özelliği sağlar. Dokularda üç tip epitel-mezenkimal geçiş bilinmektedir. Tip 1 embriyogenezis sırasında dokular oluşurken dermal fibroblastlarda, Tip 2 erişkinlerde remodelling ve fibrozis sırasında ve Tip 3 kanser hücreleri fenotipik dönüşümle hareketlilik kazanıp metastaz yaparken gözlenir. yara iyileşmesinde öznemli olan Tip 2 epitel-mezenkimal geçiştir. Bu geçişte yapılan moleküler incelemlerde bu geçişi sağlayan bazı mekanizmalar(Bmp, Wnt, Notch/Delta ve Hedgehog gibi) belirlenmiştir.
Yara iyileşmesinde derinin üzerinin kapanması yani epitelizasyon önemlidir. Bu yaraya bitişik epitel hücrelerinin yara merkezine doğru proliferasyonu ve migrasyonu ile ilişkilidir. Yaralanmanın 1. günü yara kenarındaki epidermis kalınlaşır. Yara kenarındaki marjinal bazal hücreler alttaki dermise olan bağlantılarını kaybeder genişler ve geçici matriksin yüzeyine doğru hareketlenir. Yara kenarındaki hücreler hızla prolifere olup birbirleri üzerinden hareket ederek(yara alanına doğru) yara defektini kapatırlar. Bu süre hafif yaralarda 48 saatte tamamlanır ancak daha büyük defektli yaralarda bu süre uzar. Bu sürecin kontakt inhibisyon kaybı ile fibronektin ve immün monomoleküler hücrelerden salınan sitokinlerce kontrol edildiği bilinmektedir. Özellikle EGF, TGF-Beta, PDGF ve IGF-1 bu sitokinlerin başlıcalarıdır.
Patolojik Yara İyileşmesi
Fizyolojik yara iyileşmesindeki hücresel ve yapısal kusursuz etkileşim, çeşitli faktörler ile bozulabilir ve patolojik yara iyileşmesi gelişir. Patolojik yara iyileşmeleri, bozulmanın oluşma nedenine ve iyileşmedeki zamanlamasına bağlı olarak kalıcı, kronik yaralar ve patolojik skarlaşma şeklinde ortaya çıkmaktadır.
İyileşmeyen kronik yaralar klinik olarak yaygındır ve esas olarak yara iyileşmesinin inflamatuar ve proliferatif fazlarındaki bozukluklarda görülür. Başlıca nedenler arasında, kronik inflamatuar aktiviteyi sürdüren ve yara iyileşmesinin sonraki aşamalarına geçişi engelleyen enfeksiyonlar ile yaradaki yabancı cisimler yer almaktadır. Ayrıca, ödem (artmış doku basıncı) ve dolaşım bozuklukları, doku yetersiz beslenmesine ve oksijenizasyonuna yol açarak yarada yetersiz beslenmeye neden olmaktadır.
Patolojik yara izlerinin gelişimine temel olan, anabolik ve katabolik süreçler arasındaki dengesizliktir. Yara iyileşmesinin erken evrelerinden sonra artan inflamatuar aktivitenin (lokal ve sistemik) devam etmesi kritik bir faktördür. Proinflamatuar sitokinlerin salınımının uzaması dokuya makrofajları çeken büyüme faktörlerinin salınımının devamına yol açar. Bunlar dokuda miyofibroblastlara farklılaşan ve fibrotik yeniden şekillendirme, fibrozis süreçlerini kontrol eden fibroblastları aktive eder. Patolojik yara iyileşmesinde inflamatuar süreçlerin rolünü daha iyi anlamak için fetusta yara iyileşmeleri araştırılmıştır. Fetüste yara iyileşmesinin skarlaşmadan ilerlediği gösterilmiştir. Fetusta yara iyileşmesinde önemli ölçüde daha az inflamatuar süreç vardır ve daha az proinflamatuar sitokin (IL-6/IL-8) salınır. Bu, miyofibroblastların aktivasyonunun önemli ölçüde azalmasına ve fibrozisin ideal oranlarda oluşmasına yol açar.
İnflamatuar süreçlere ek olarak, bozulmuş yeniden şekillendirme süreçleri de söz konusudur. Bunlar, kolajenazların azalmış aktivitesinden ve apoptoz eksikliğinden kaynaklanır. Bu süreçler aşırı ve ilerleyici fibroza yol açar. Ayrıca, TGF-β1 ve TGF-β2 artışı (fibroblastların çoğalması, keratinosit çoğalmasının inhibisyonu, miyofibroblastların farklılaşması, matris materyalinin birikmesi) ve aşırılığı patolojik skarlarda ifade edilmektedir.
Lokal faktörlerin yanı sıra sistemik faktörler de yara iyileşme bozukluklarının patogenezinde rol oynar. Etkileyen sistemik önemli bir faktör hastanın yaşıdır; çünkü yaşla birlikte kolajen sentezinin kalitesi azalır.

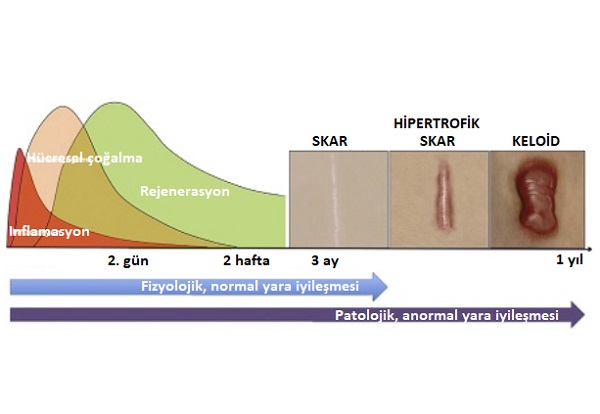
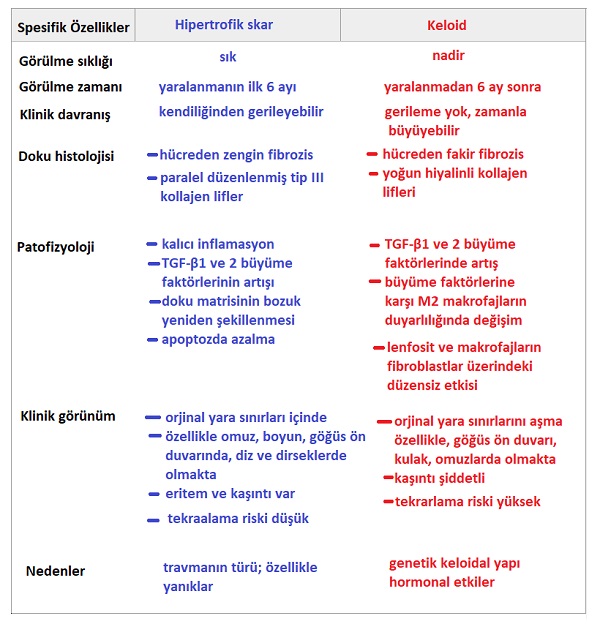
Yara iyileşmesinin rejeneratif fazı, görünür bir yara izinin normal bir skarın oluşumunun ötesine geçer; patolojik skarlar oluşmaktadır. Patolojik yara iyileşmesi, yara dokusunun aşırı üretimi ile sonuçlandığında hipertrofik skar ve keloid oluşur. Her ikisinde de yara dokusunun aşırı üretimi söz konusu olmakla birlikte, ayrımları çok iyi yapılmalı ve spesifik özellikler iyi bilinmelidir.
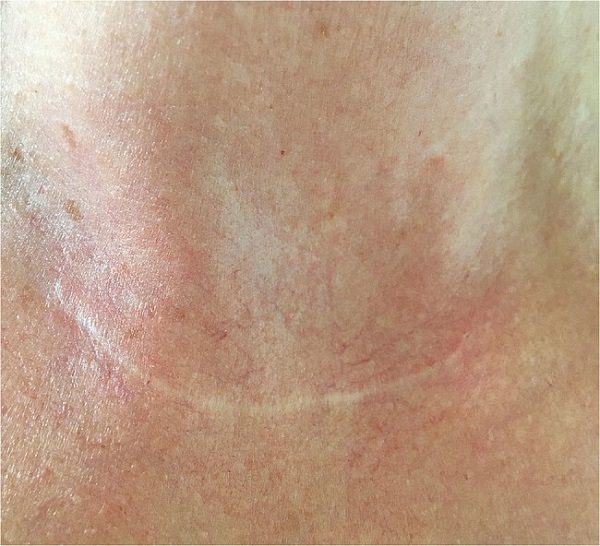
Hipertrofik skarlar
Orijinal yaranın sınırları içinde kalan deriden kabarıklıklar gösteren patolojik skarlardır. Genellikle fizyolojik yara iyileşmesinin zaman dilimi içinde, yaralanmadan 6 aydan kısa bir sürede oluşurlar ve zamanla kendiliğinden gerileyebilirler. Lokal kaşıntı ve eritem görülmektedir. Komplikasyonları arasında fonksiyonel kısıtlamalara yol açan doku çekilmeleri yapan sert doku bantları, kontraktürler bulunabilir. En sık görülen nedenler arasında aşırı bir inflamatuar yanıta neden olan ve patolojik yara iyileşme koşullarının gelişimini destekleyen ısıya bağlı yanıklar yer almaktadır. Termal travmanın %90'ından fazlası, defektin derinliğine bağlı olarak hipertrofik skarlarla sonuçlanır. Hipertrofik skarları fizyolojik yara iyileşme süreçlerinin istenmeyen bir sonucu olarak düşünebiliriz. Fizyolojik yara iyileşmesine göre hipertrofik skarlarda önemli miktarda fibroblast fazlalığı düşünülebilir. Bozulmuş Th2 tepkisi ile artan inflamatuar aktivite, yeniden şekillendirme süreçlerini ve dolayısıyla hücre dışı matris (ECM) üretimini etkiler. Yara iyileşmesindeki doku sentezi (artmış fibroblast aktivitesi, artmış fibronektin üretimi, artmış kolajen tipleri I ve III üretimi, artmış TGF-β1 ve 2) ve doku yıkımı (azalmış kolajenaz aktivitesi, azalmış apoptoz) arasında bir dengesizlik söz konusudur. Artmış proteoglikan seviyeleri ve azalmış dekorin seviyeleri ile değişen kompozisyon, hipertrofik skarların gelişiminden kısmen sorumlu olabilir. Aynı zamanda, doku matrisinde ilerleyici yeniden şekillendirilmesi, hipertrofik skarların kendiliğinden gerilemesine katkıda bulunabilir. Bu süreçte apoptotik süreçler de yer alır. Histolojik korelasyon, paralel demetler halinde düzenlenmiş çok sayıda kolajen lif (tip III) içeren hücre açısından zengin bir konglomeradır. Keloidlerin histolojik farklılaşması için α-SMA ekspresyonunun önemi tartışmalıdır.
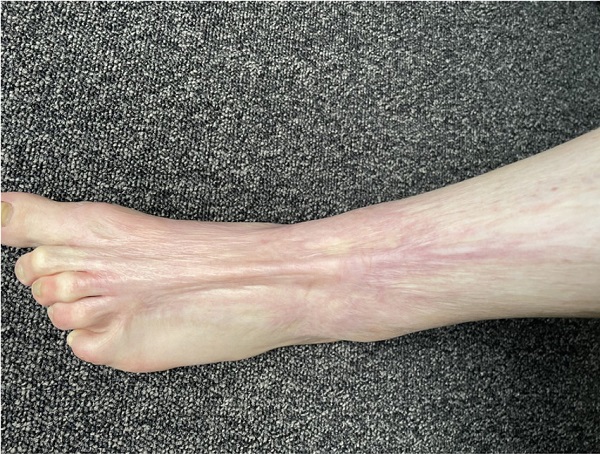
Keloidler
Hipertrofik skarların aksine, keloidlerde skarlaşma orijinal yaralanma alanının dışına taşacak şekilde büyüme ile karakterizedir. Keloidler klinik olarak bazen şiddetli kaşıntı, yanma ve ağrı hissi ile birlikte olmaktadır. Klinik görünümleri, yara alanında deriden belirgin kabarma gösteren fibrotik bir doku görünümündedir. Orijinal yaralanmadan 6 ay ila yıllar sonra ortaya çıkabilmektedir. Sıklıkla yerleşim alanları omuz kuşağı, göğüs ön kısmı ve kulaklardır.
Kadınlar ve erkekler arasında görülme sıklığı eşit olmakla birlikte, renkli insanlarda ve Asyalı nüfusta görülme sıklığı çok fazladır. Bu özellikleri ve ailesel kümelenme göstermesi, genetik bir ilişki olduğunu düşündürmektedir. Ek olarak, ergenlik ve gebelik sırasında görülme sıklığında artış göstermesi, hormonal bir etkinin olabileceğini desteklemektedir.
Hipertrofik skarların aksine, keloidal dokuda histolojik olarak zayıf hücre proliferasyonu ve hiyalinli tip I kollajenli bağ dokusunun artışı görülmektedir. Hipertrofik skarlar fizyolojik yara iyileşmesi sırasında uzun süren bir inflamatuar süreç ile ortaya çıkarken, keloidler doku travmasından aylar sonrasına kadar oluşmamaktadır. Bu geç klinik gelişim, doku hasarını yapan faktörlerden bağımsız olarak spesifik bağışıklık tepkisinde bir patolojik skarlaşma olduğunu göstermektedir (lenfositle ilişkili sitokinler, fibroblast aktivitesindeki değişikliklere katkıda bulunabilir). Keloid skar dokusunda çok sayıda inflamatuar hücre tespit edilebilir ve bunlar büyüme faktörlerinin artan salınımını kontrol eder. Fibroblastlar, TGF-β ve trombosit kaynaklı büyüme faktörüne (PDGF) karşı daha yüksek duyarlılık gösteren büyüme faktörü reseptörlerinin artışı ile daha fazla doku proliferasyonuna yol açar. M2 makrofajlarla ilişkili genlerin keloidlerde daha fazla olduğu ifade edilmektedir ve fibroblastlar giderek daha fazla dokuda birikmekte ve büyüme faktörlerinin artan miktarı ile miyofibroblastlara dönüşmektedir. Mekanotransdüksiyon uyarı yollarının yara dokusu ve çevresinde aktivasyonu, yara sınırlarının ötesinde keloidlerin gelişimini açıklayabilir. Yetersiz tedavilerle yüksek tekrarlama oranı, keloid dokuda hafıza T hücrelerinin artan varlığıyla ilişkili olabilir.
Patolojik skarlarda tedavi
İster hipertrofik skarlar ister keloidler olsun, skarların tedavisi için medikal nedenlerimiz; skarın neden olduğu fonksiyonel kısıtlamalar ve kalıcı mekanik tahrişlerdir. Örneğin, dirsekte yanık sonrası gelişen patolojik hipertrofik skar, kolun hareketlerini kısıtlayabilir. Çok fazla kaşıntı veya ağrı gibi semptomlar, bu tür skarlar için tedavi nedeni olabilir.
Patolojik skarlarda tedavi için bir diğer neden, hastanın estetik problemleridir. Skarların ve özellikle keloidlerin, hastaların yaşam kalitesini estetik olumsuzlukları ile sınırlayabileceği, hatta kendilerini damgalanmış gibi hissedebilecekleri akılda tutulmalıdır.
Tedavinin hedefleri, tedavi öncesinde hasta ile bireysel olarak tartışılmalıdır. Hastanın beklentilerinin açıklığa kavuşturulması ve skardaki estetik beklentilerinin tartışılması son derece önemlidir. Tedavi sürecinin takibi ve amaçlanan hedeflerin izlenmesi için tedavi öncesi ve sonrasında fotoğrafik dokümantasyon önerilmektedir. Semptomlar (kaşıntı, yanma, ağrı, deriden kabarıklık, skarın sertliği gibi) özel derecelendirme skorları ile kayıt altına alınmalıdır (Vancouver Yara İzi Ölçeği (VSS) veya Hasta ve Gözlemci Yara İzi Değerlendirme Ölçeği (POSAS) gibi). Tedavi sonuçları üç ila altı tedavi sonrası (yaklaşık üç ila altı ay sonra) değerlendirilebilir. Subjektif hasta memnuniyetinin sağlanması, tedavinin bir başarısı olarak kabul edilir.
Hipertrofik skarlarda tedavi basamakları;
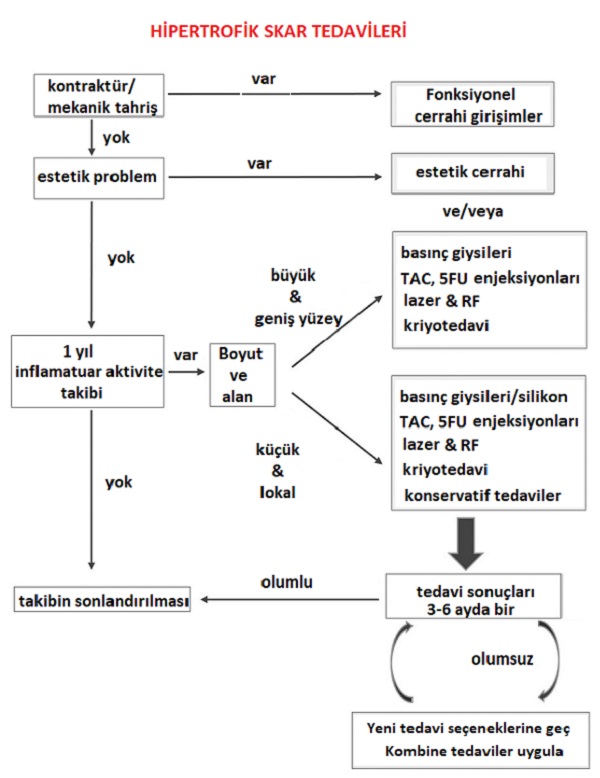
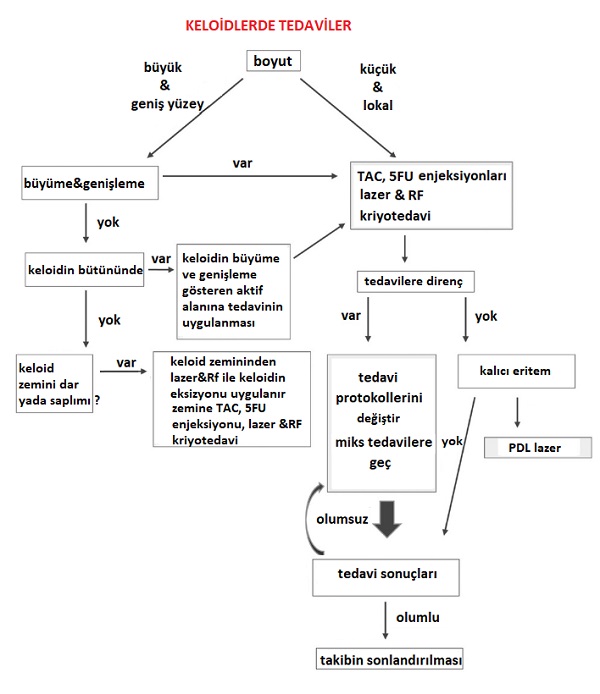
Keloidlerde tedavi basamakları;