- Gösterim: 2744
Diyabet kaynaklı kronik cilt yaraları yüksek oranda tıbbi zorluklar yaratmakta; iyileşmeyen yaralar, enfeksiyon riskleri, kötü yara iyileşme riskleri ve günlük aktivitelerin kısıtlanması gibi. Cilt yaralarında yaranın içindeki ve çevresindeki mikroçevre yara iyileşmesi için uygun bir koşul sağlayarak karmaşık bir iyileşme sürecini düzenler. Bu mikroçevrede iyonik ortam ve bu iyonlardan oluşan pH değeri önemli faktörler arasında yer almaktadır. pH ve iyon konsantrasyonları kronik diyabetik yaraların iyileşmesindeki yüksek orandaki zorluğun nedenleri arasında tanımlanmaktadır. Kronik ve iyileşmesi uzamış yaralarda farklı yara pansumanları yaralardaki pH, kalsiyum (Ca 2+), sodyum (Na +), potasyum (K +) konsantrasyonları ile gümüş (Ag +), bakır (Cu 2+), demir (Fe 2+/Fe 3+), çinko (Zn 2+) ve magnezyum (Mg 2+) gibi metal iyonlarına odaklanmaktadır.
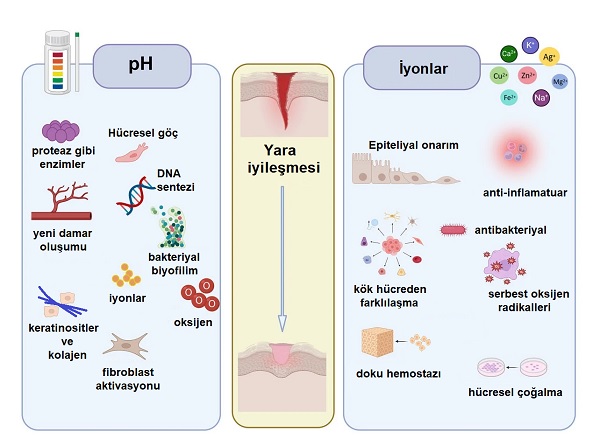
Şeker hastalığında (diabetes mellitus; DM) cilt yaraları yüksek tekrarlama oranları ve kötü iyileşme süreçleri ile önemli bir komplikasyondur. Dokularda yara iyileşmesi; pıhtılaşma, inflamasyon, dokuda hücrelerin çoğalması ve yeniden yapılandırılması aşamalarını içeren, birbirini takip eden karmaşık bir süreçtir. Diyabet kaynaklı ciltte dolaşım sistemindeki yetersizlikler, cildin iyileşme süreci boyunca sınırlı oksijen temini ve yüksek oksijen tüketimi ile sonuçlanır; bu da ciltte uzamış inflamatuar yanıtla sonuçlanmakta ve ciltte yara iyileşmesinin uzaması ve sorunlu olması anlamına gelmektedir. Diyabet kaynaklı yüksek glikoz seviyeleri yarada vasküler endotelyal büyüme faktörü (VEGF) ve hipoksi indükleyici faktör-1α'nın (HIF-1α) aktivitesini azaltmaktadır. Ciltte birçok önemli proteinin enzimatik olmayan glikozilasyonu artarak ciltte anormal hücre ve hücreler arası destek dokunun (hücre dışı matris; ECM) fonksiyonlarına neden olmaktadır. Tüm bu olumsuzluklar yarada yetersiz yeni damar oluşumu ve doku hemostazı ile sonuçlanarak yara iyileşmesini geciktirmektedir. Son yıllarda yara iyileşmesini desteklemek üzere tasarlanan hidrojeller, köpükler, hidrokolloidler, nanofiberler, süngerler ve yarı geçirgen membranlar gibi çok işlevli biyomalzemelerin geliştirilmiştir.
Cildin bütünlüğü bozulduğunda, yara geliştiğinde yara içerisinde ve çevresinde bir mikroçevre oluşmakta. Yara mikroçevresinin “dış mikroçevre” ve “iç mikroçevre” olarak ikiye ayrılabileceği ileri sürülmüştür. Dış mikroçevre, yaranın hemen bitişiğindeki cilt alanı olarak tanımlanırken iç mikroçevre ise yara yüzeyinin hemen altında ve bitişiğinde alnı tanımlar. Cildin çeşitli hücreleri ve hücre dışı destek dokusu (ECM) iç mikroçevrede, yara içerisindeki bakteri yükü, diğer mikroorganizmalar, pH, iyonlar, oksijen, sıcaklık, nem, ışık dış mikroçevrede kritik öneme sahip faktörlerdir. Bu faktörler yaranın içinde/çevresinde spesifik ve karmaşık bir sabit durum yaratarak yara iyileşmesinin dinamik süreci için koşullar sağlamaktadır. Dinamik mikroçevre cildin hemostazını korurken yara iyileşmesi yönünde hücre aktivitelerini doğrudan veya dolaylı olarak düzenler. Dış ve iç mikroçevre sürekli olarak birbirleriyle alışveriş içerisindedir ve birbirlerinden etkilenirler.
Cilt hemostazında cilt pH'ının önemi fark edildikten sonra cilt yaralarının pH'ına odaklanılmış ve yara iyileşmesini etkileyen önemli bir faktör olduğu vurgulanmıştır. Bu nedenle cilt pH'ını belirleyen iyonik ortam sağlayıcı kalsiyum (Ca²⁺), sodyum (Na⁺), potasyum (K⁺) ve bakır (Cu²⁺) ile demir (Fe²⁺/Fe³⁺), gümüş (Ag⁺), çinko (Zn²⁺) ve magnezyum (Mg²⁺) gibi metal iyonları da yara iyileşmesinde son derece önemlidir. Bu iyonlar bağışıklık ortamı için çok önemlidir. Doğuştan gelen bağışıklık uyarımı ve T hücresi aktivasyonunda metal iyonları aracılık etmektedir. İyonlar oksidatif fosforilasyon, ATP üretimi, mitokondriyal bütünlük, mitokondriyal hacim, enzim aktivitesi, sinyal iletimi, çoğalma ve apoptozis dahil olmak üzere hücresel metabolizma için kritik öneme sahiptir.
Cilt dokusundaki Ca²⁺, Na⁺, K⁺, Cu²⁺, Fe²⁺/Fe³⁺, Ag⁺, Zn²⁺, Mg²⁺ ve diğer iyon içerikleri kan plasması tarafından sağlanır. Bunlar cildin hemostazını sağlarken yara iyileşmesini etkileyen iyonik ortamı oluşturur. Yaranın iç ve dış mikroçevresi arasında iyonların dinamik değişiklikleri yara iyileşmesini farklı aşamalarda etkiler. Hiperglisemik ortam, dokunun yetersiz kanlanması kaynaklı hipoksi ve inflamasyon cilt dokusunda anormal bir iyonik ortama neden olabilir ve buda yara iyileşme sürecini etkileyerek uzmanış yara iyileşmesine neden olmaktadır.
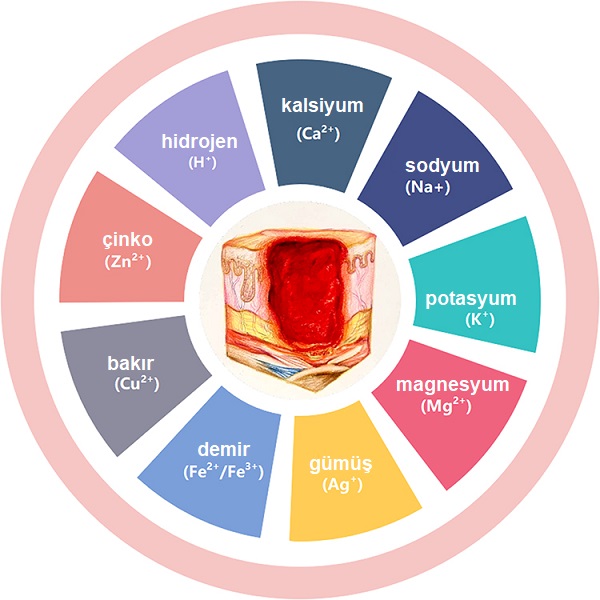
pH, herhangi bir dokuda sıvı çözeltisinde hidrojen iyonlarının (H+) termodinamik aktivitesinin ters logaritmik ölçüsüdür. H+ konsantrasyon değeri genellikle pH değeri olarak bilinir. Büyük bir pH değeri daha düşük bir hidrojen iyonu konsantrasyonunu gösterir. Ciltte keratinositler tarafından sentezlenen ve hücre dışına salgılanan organik asitler H+ konsantrasyonunu belirler. Normal cilt yüzeyinin pH'ı 4,8 ile 6,0 arasında değişmektedir. Bu asidik pH, stratum korneumdan dermise doğru artarak 6,8'e yükselir. Cildin pH değeri anatomik alana, cinsiyete, yaşa veya ırka dayalı önemli farklılıklar göstermektedir.
Cilt bütünlüğü bozularak yara oluştuğunda hasarlı kılcal damarlardaki alkali plazma dokuya sızmakta, yaradaki pH önemli ölçüde artmaktadır. Yaranın erken evresinde mikroçevresinin pH'ı yaklaşık olarak nötr olup ortalama değeri 7,44'tür. Ancak bu pH yara iyileşme süreci boyunca sürekli değişir. Yara iyileşmesinin pıhtılaşma veya inflamatuar aşamasında yara mikroçevresinde kan dolaşımı azalmakta, yaraya önceki kan akımı azalmaktadır. Bu azalmadan kaynaklanan doku karbondioksit stazı, glikolizinin anaerobik reaksiyonu ile laktik asit üretimi artışı pH'ı düşürmektedir. Yaranın inflamatuar fazının sonuna göre nekrotik doku temizlenir, doku kan akımı tekrar sağlanır, glikozun aerobik reaksiyonu ile pH tekrar artmaktadır. Yara iyileşmesinin sonraki aşamasında; yara epitelizasyonu ve redüksiyonu, stratum korneumun yeniden yapılması ile pH nötr hale gelir. Sonrasında yara dokusunun oksijen ihtiyacı artmakta, yara dokusunda glikoliz ve laktik asit üretimi olmakta, yara kenarında epitel sekresyonu artmakta ve yara pH'ının tekrar düşmektedir. Ayrıca, yara merkezinin pH'ı tüm yara yüzeyine göre her zaman daha yüksektir.
Kronikleşmiş yaralarda ise pH değişimi bu normlardan farklılık göstermektedir. Akut yaralarla karşılaştırıldığında, kronik diyabetik yaralar nispeten alkali bir ortama sahiptir; pH 7,42 ile 8,90 arasında değişmektedir. Kronik diyabetik yaraların pH'ı 9,25 kadar çıkabilmektedir. Bu kapanmayan yarada kan plasma ve hücreler arası interstisyel sıvının dış ortama maruz kalmakta ve üre enzimi aracılığıyla üre kaynaklı amonyak salınımı olmakta, bunlar ciltte daha alkali bir pH'a yol açabilmektedir. Kronik diyabetik yaralarda yara yüzeyinde epitelizasyon olduğunda pH tekrar asidik hale gelir. Kronik diyabetik yaraların pH'ının artması proteaz enzim seviyesinde artışa, metalloproteinaz doku inhibitörlerinin (TIMP) azalmasına, reaktif oksijen türlerinin (ROS) artmasına ve enfeksiyona yol açmaktadır. Bu biyokimyasal dengesizlikler fibroblast aktivitesinin azaltmakta. Bu süreçler yara iyileşme süreci için gerekli olan hücreler arası detek dopkunun bileşenlerinin yok edildiği anormalliklerine yol açabilmektedir. Kronik diyabetik yaralarda bu olumsuz süreç uzun süreli inflamasyona, hasarlı ve defekli yara iyileşmesine neden olmaktadır.
Yara mikroçevresinin pH'ı, yara iyileşmesi sırasında tüm biyokimyasal reaksiyonları dolaylı veya doğrudan etkiler.
- Yaradaki H+ konsantrasyonu, dokuda proteinleri parçalayan, proteolitik enzim olan proteaz aktivitesini doğrudan etkiler. pH'ın 8'den 4'e düşmesi, proteaz aktivitesini %80 oranında azaltabilir.
- Dokudaki oksijen içeriği yara iyileşmesini doğrudan etkilemektedir. Dokuda oksijen 40 mmHg'den fazla olduğunda iyileşme mümkün olmaktadır. Dokuya oksijenin taşınması hemoglobin (oksihemoglobin) ile sağlanır. Asidik bir ortamda, oksijenli hemoglobin tarafından salınan oksijen seviyesi artar. Örneğin, pH 0,60 azaltıldığında, oksihemoglobinden oksijen ayrışması %50 artar; pH 0,90 azaltılırsa, oksihemoglobinden oksijen ayrışması 5 kat artmaktadır.
- Yara dokusunda mikroorganizmalar kendi ekolojik ortamlarını yaratırlar ve bu da biyofilm olarak tanımlanır. Biyofilmler kronik yaraların %60-100'ünde bulunur. İnsanda patojenik bakterilerin büyümesi için pH'ın 6,0'dan büyük olması gerekmektedir. Bu nedenle asidik bir ortam, düşük pH patojen mikroorganizmaların büyümesini engeller. Buna karşın alkali yara mikroçevresinde bakteriyel enfeksiyonlar ve biyofilmler kolayca oluşur. Ayrıca yara mikroçevresinde mikroorganizmaların kolonizasyonu yara dokusunu alkali hale getirmektedir. Bu kısır döngü yaratırken alkali ortam yara iyileşme zorluklarının nedenlerinden birisi haline gelmektedir.
- Yara iyileşmesinin yeni damar oluşumu, anjiyogenez ve hücresel çoğalma aşamasında asidik yara mikroçevresinin gerektiği bilinmektedir (artmış transforme edici büyüme faktörü [TGF]). pH 7,50'den büyük olduğunda, yara dokusuna hücre göçü ve DNA sentezi artmaktadır. Asidik bir ortamda, fibroblastlar (trombosit kaynaklı büyüme faktörü [PDGF] salınımıyla artar) ve keratinositler aktif olarak çoğalır ve yaranın yüzey alanının küçülmesini sağlayan miyofibroblastların aktivitesi, kontraktiliteleri artmaktadır.
- Antibiyotiklerin yara dokusunda etkinlikleri pH ile değişmektedir. Bir aminoglikozit antibiyotik olan gentamisin aktivitesi, pH 5,50'ye kıyasla pH 7,80'de 90 kat daha fazla etkinlik göstermektedir. pH'daki azalma gümüş iyonlarının aktivitesini, yani antibakteriyel etkilerini artırabilir. Kronik yaralarda bakteriyel biyofilmler içerdiğinden ve antibiyotiklerle klinik müdahale gerektirdiğinden, ilaçların etkilerini artırmak için yara mikroçevresinin pH'ı dikkate alınmalıdır.
- pH'ı düşürmek ve daha asidik bir ortam yaratırken bakterilerden kaynaklanan üreazın etkisiyle üreden salınan amonyak gibi son ürünler ve bunların dokuda toksisiteleri azalmaktadır. Amonyak yara dokusu için toksiktir ve yara iyileşmesine elverişli olmayan alkali bir ortam yaratır.
Günümüzde yaraların pH'ı, düz cam elektrotlu bir pH metre veya pH turnusol kağıdı kullanılarak klinik olarak ölçülebilir. Ancak, turnusol kağıdı değerlendirmelerinde sonucu belirleyen renklerin yorumlanmasında farklılıklar vardır ve bu da yanlış sonuçlara yol açabilir. Ayrıca, hasta yaralarına temas eden pH metre elektrotlarının ve turnusol kağıtlarının steril olması zorunluluğu bulunmaktadır. Kronik yaralarda pH düzenleyici tedavi yaklaşımı kullanılabilir, ancak hala bazı sorunlar içermektedir. Öncelikle yaraların alkali mikroçevresinin asitlendirilmesinin sürdürülebilir olması gerekmektedir. Bunun için asidik ilaçların veya yara pansuman içeriklerinin düzenli değiştirilmesi gerekmektedir. Ayrıca yaranın iyileşme evresine göre pH'daki dinamik değişimler dikkate alınmalıdır. pH ayarlanırken epitel rejenerasyon hızı, granülasyon büyüme koşulları ve ilaç etkinliği değişiklikleri dahil olmak üzere birden fazla faktör dikkate alınmalıdır.
Son yıllarda yaraları tedavi etmek için antibakteriyel ajan olan birçok asit kullanılmıştır. Bunlar içerisinde yaygın olarak kullanılanı; vücutta doğuştan gelen bağışıklık süreci tarafından üretilen, yaralardan döküntüleri ve mikroorganizmaları temizleyebilen doğal olarak oluşan hipokloröz asittir. Yaygın olarak kullanılan bir diğer asit ise sitrik asittir. Ayrıca, yara asitlenmesi bağlamında asetik asit, borik asit, sitrik asit, askorbik asit, aljinik asit, hyaluronik asit ve diğer asitler yara iyileşmesini belirgin etkilerle kullanılmaktadır.
Kronik Diyabetik Yaraların İyonik Ortamı
Ca 2+ ve Kronik Diyabetik Yaralar
Yaralarda Ca 2+ Değişimleri
Ca 2+ iletimi, hasarlı hücreler tarafından salınan ATP tarafından başlatılan ve çevredeki hücrelerden sitoplazmik Ca 2+ artıran en erken yara sinyalleme olaylarından biri olduğu düşünülmektedir. Cilt homeostazisi sırasında, Ca 2+ konsantrasyonu dış granüler tabakada zirve yapar ve bazal tabakada en düşük seviyededir. Cilt hasarından hemen sonra, Ca 2+ yara yatağında tespit edilebilir ve pıhtılaşma sürecini kolaylaştırır. Ca 2+ artışı, yara oluşumundan sonra 5 gün sürer ve maksimum inflamatuar aktivite ile örtüşür. Yaradaki Ca 2+ konsantrasyonu, iyileşme sürecinin ilerlemesiyle dinamik olarak değişir. Hücre dışı Ca 2+ konsantrasyonunun, yaralanmanın başlangıcından sonra inflamatuar ve proliferatif aşamalarda devam ettiği ve ardından yeniden şekillenme aşamasında azaldığı gösterilmiştir. Yara oluştuktan sonra, cilt dokusundaki Ca 2+ konsantrasyonu artar ve en yüksek konsantrasyon normal cilttekinin 60 katından fazlasına ulaşabilir. Ayrıca, yaradaki hücreler, yara iyileşmesi için gereken hücrelerin normal yaşam ortamını sürdürmek için düşük bir Ca 2+ konsantrasyonunu korurken sürekli olarak fazla Ca 2+'yi uzaklaştırmalıdır. Geçici reseptör potansiyeli vanilloid (TRPV), memeli deri dokularında yaygın olarak ifade edilen kalsiyum geçirgen, seçici olmayan bir katyon kanalıdır ve Ca 2+'nin transmembran seviyelerini ve hücrelerin depolarizasyonunu düzenler. TRPV1, TRPV2, TRPV3 ve TRPV4 kanalları bazal ve supra-bazal keratinositlerde ifade edilir. TRPV1 ve TRPV3 kanalları hücre ölümüyle ilişkilendirilirken, TRPV1 kanalları mitokondriyal hasarı ve Ca 2+ girişini indükler. Ayrıca, TRPV3, kalsiyum/kalmodulin bağımlı protein kinaz II ile indüklenen nükleer faktör kappa-B yoluyla keratinosit proliferasyonunu teşvik eder. TRPV2 kanalı büyüme faktörü-β1 ve düz kas aktin aracılı kasılmaları uyarır, sonuçta dermal fibroblastların kasılmasına yol açarak skar oluşumunu etkiler. Bu arada, TRPV4 kanalları Rho aracılı süreçler yoluyla aktin bağlantılarının organizasyonunda rol oynar. Ancak kronik diyabetik yaralardaki Ca 2+ değişimleri akut yaralardaki değişimlerden farklıdır.
Kronik Diyabetik Yaralarda Ca 2+
Anormal hücresel Ca 2+ homeostazisi ve sinyalizasyonu T1DM ve T2DM'nin ortak bir özelliğidir. Bu anormallikler tipik olarak artan dinlenme Ca 2+ seviyeleri, azalan Ca 2+ taşıyıcı aktivitesi ve azalan uyarım kaynaklı Ca 2+ sinyalizasyonu ile ortaya çıkar. Yüksek glikoz koşulları altında keratinositlerdeki hücre içi ve hücre dışı Ca 2+ konsantrasyonlarındaki artış, membran depolarizasyonuna neden olabilir ve hücre membranının ve lameller gövde ekzositozunun içe doğru hareketini bozabilir, böylece hücreler arasında tabakalı bir lameller membran oluşumunu etkiler ve cilt bariyeri onarımını geciktirir.
Yara iyileşmesinde pH sonrası iyonlar ve etkilerinden bahsedilmelidir.
- Kalsiyum, Ca 2+'nin etkileri; yara sinyalleme aktivitesinde ve yara iyileşmesinin düzenlenmesinde önemli bir rol oynar.
- Yara oluşumunda kan pıhtılarının oluşumunda, ilk pıhtılaşma fazında rol oynar. Faktör IV olarak da bilinen Ca 2+, diğer pıhtılaşma faktörleriyle birlikte, pıhtılaşma sürecini tetikler, trombin sentezini hızlandırır ve erken fibrin oluşumunu destekler.
- Yaranın iltihaplanma fazında hücre dışı Ca 2+ nötrofillere girerek nötrofilik fonksiyonları düzenler.
- Yaranın epitel iyileşme sürecinin başlatılması ve desteklenmesinde görev almaktadır. Hücre dışı Ca 2+ epidermal homeostazın önemli bir düzenleyicisidir; epidermal hücre içi kalsiyum E-kadherin aracılı sinyallemeyi indükleyerek epitel iyileşmeyi başlatır ve nihayetinde keratinosit yapışmasını, farklılaşmasını ve hayatta kalmasını teşvik etmektedir.
- Ca 2+ keratinositlerin farklılaşmasını düzenleyerek stratum korneumda keratinosit farklılaşmasını ve çoğalmasını sağlayarak cilt bariyerinin oluşumu için önemlidir. Keratinosit çoğalması hücre dışı Ca 2+ konsantrasyonuyla ters orantılıdır; düşük Ca 2+ konsantrasyonlarında daha hızlı hücre çoğalması ve yüksek Ca 2+ konsantrasyonlarında daha yavaş hücre farklılaşması olur. Yaradaki yüksek Ca 2+ konsantrasyonları keratinositlerin çoğalmasını ve göçünü engeller ve yara iyileşmesini geciktirdiğine inanılır.
- Ca 2+ anjiyogenezde yer alan çoklu sinyal yollarını düzenleyen önemli bir sinyal molekülüdür. Endotel hücrelerine Ca 2+ girişi, göçlerinde, yapışmalarında, çoğalmalarında ve anjiyogenezlerinde önemli bir rol oynar. Yaradaki daha yüksek Ca 2+ konsantrasyonları kolajen sentezini ve kan damarı oluşumunu artırabilir.
- Fibroblastlar hücresel kasılma için hücre içi Ca 2+ kullanır. Böylece hücre içi bağlantılarda aktin yeniden şekillenmesini ve kaderin toplanmasını sağlayarak yaraların boyutunu küçültmeye yardımcı olur. Hücre dışı Ca 2+ takviyesi hücre metabolik aktivitesini, göçünü, matriks metalloproteinaz (MMP) üretimini, kolajen sentezini, sitokin salınımını artırır ve hücre kasılmasını azaltır.
- Ca 2+ ayrıca protein ve lipid açısından zengin olan epidermal bariyerin işlevlerini korur.
- Ca 2+ cildin doğuştan gelen bağışıklık sisteminde önemli oyuncuları olan doğal öldürücü (NK) hücrelerinin birincil aktivatörlerinden biridir. Diyabetli bireyler NK hücre aktivitesindeki kusurlara eğilimlidir ve bu da sonuçta enfeksiyon riskinin artmasına yol açar. NK hücreleri yarada aktive olduğunda sitotoksik etkiler gösterir, bağışıklık düzenleyici sitokinler IFN-γ ve TNF-α üretir, makrofajları ve diğer bağışıklık hücrelerini aktive eder. Aktive edilmiş makrofajlar yara debridmanına katılır ve yara iyileşmesinde rol oynayan temel düzenleyici faktörlerdir.
Yara yüzey tedavilerinde kalsiyum içeren pansuman uygulamaları oldukça sık kullanılmaktadır; kalsiyum aljinatlar, kitosan kalsiyum aljinatlar, kalsiyum fosfatlar gibi. Bu ürünler yara yüzeyine uygulandığında Ca 2+ açığa çıkarak bağışıklık yanıtını destekleyerek yara epitelizasyonunu ve iyileşmesini hızlandırabilmekte, bakteriyostazı artırırken fibroblastların göçünü, kollajen sentezini ve sitokin salınımını artırabilmektedir.
- Na + /K +'un etkileri;
- Na + vücuttan ter yoluyla atılır. Ozmotik tamponlama ve termoregülasyonda rol oynar. Ciltte Na + epidermiste eşit bir dağılım gösterir. Bu dağılımda ter önemli bir kaynaktır ve terleme sırasında cildin stratum korneumundaki Na + miktarı artar. Ciltte stratum korneum hariç tüm epidermal tabakalarda hücrelerde sodyum kanalları bulunmaktadır. Bu kanallar farklılaşmış keratinositlerde artarken ve sodyum homeostazının korunmasında önemli bir rol oynarlar. Yara iyileşmesinin olgunlaşma aşamasında(epitelizasyondan sonra), deri bariyeri işlev bozukluğu genellikle yara dehidratasyonu nedeniyle Na + düzensizliğine yol açar ve sonuçta kronik inflamasyona neden olur.
- Deride, K + keratinositlerin terminal farklılaşmasını ve kütikül bariyer fonksiyonlarını düzenleyerek yara iyileşmesinde rol oynar. Ca 2+ 'nin aksine, K + seviyeleri epidermisin spinosum tabakasında zirveye ulaşır ve granüler tabakada en düşük seviyelerine düşer. K + kanalları hücre dışı artan Ca 2+ konsantrasyonuna yanıt olarak aktive olur. Bu nedenle, deri bariyerinin bozulmasından sonra Ca 2+ seviyelerinde bir artış K + 'da bir artışa yol açar. Hücre içi ve dışı potasyum oranlarının korunmasında potasyum kanalı Kcnh2 ve Kcnj8 rol oynamaktadır. Kcnh2, K + 'yi hücrenin dışına ileterek plazma membranını hiperpolarize ederek keratinositleri koruyan bir potasyum kanalıdır. Kcnj8 kanalları, membran potansiyeli depolarizasyonunu koruyan içe doğru potasyom geçişini sağlayan K + kanallarıdır. İlginçtir ki, Kcnj8 aktivasyonu ve Kcnh2 inhibisyonu yara iyileşmesini destekler.
- K + keratinositlerin farklılaşmasını engelleyebilir ve Ca2 + giriş hızını artırabilir.
- Na/K pompası aracılı transepitelyal potansiyel (TEP) oluşumu ile ilgili olarak, yara elektrik alanı yara iyileşmesi için en önemli yönlendirici sinyal olarak kabul edilir. TEP üzerinden yara elektrik alanının yoğunluğunu kontrol edilerek yara iyileşmesi desteklenir. Ciltte Na/K pompaları TEP'i oluşturmak pompa molekülü bir ATP molekülünün hidrolizi ile üretilen enerjiyi kullnarak üç Na + iyonunu hücre dışına iki K + iyonunu hücre içerisine almaktadır. K + keratinositlerin farklılaşmasını engelleyebilir ve Ca2 + giriş hızını artırabilir.
Yara tedavisinde Na + veya K + içeren pansumanlar dokuda ödemin azaltılması ve yara iyileşmesinin desteklenmesi için kullanımakta.
- Gümüşün, Ag etkileri; insan vücudundaki gümüş içeriği çok düşüktür (yaklaşık 2 μg/L) ve vücuda solunum, oral alım, cilt teması ve diğer yollarla alınmaktadır. Ag, sulu bir ortamla temas yoluyla iyonize olduğunda Ag+ üreten inert bir metaldir ve etkili bir antibakteriyel maddedir. 1 ppm'de Ag+'nın bakterisidal etki gösterebileceğini göstermektedir. Dahası, Ag+ geniş spektrumlu, yüksek antibakteriyel aktivite gösterebilir, bakteri, mantar ve virüslerin aktivitesini inhibe edebilir. Ag+'nın antibakteriyel mekanizması reaktif oksijen türlerinin üretimi üzerinden olmaktadır. Bakteri hücrelerine giren Ag+, önemli metabolik süreçlerde yer alan DNA ve bakteri proteinlerini yok eder ve sonuçta bakteri replikasyonunun baskılanmasına ve ölümüne neden olur. Ag+, bakteri yüzeyinin negatif yüklü yapısını, hücre zarı yapısını yok eder veya zayıflatır. Bu da bakteri ölümüne neden olur. Ag+, membran proteinlerine ve solunum zincirlerine bağlanarak bakteriyel ATP üretimi, tüketimi ve ölümünü etkiler. Ek olarak, Ag+ ciltte keratinositlerin ve fibroblastların çoğalmasını teşvik eder. Bunlara ek olarak Ag+ ve klorür iyonları AgCl oluşturmakta, bu da yara iyileşmesi için elverişli olmayan bir ortam sağlamaktadır. Bu nedenle yarada maksimum Ag+ konsantrasyonu yaklaşık 1 μg/mL olmalıdır. Ag+ inflamasyonu ve enfeksiyonu inhibe edebilir (MMP ve sitokin salınımını düzenleyerek). Gümüş bu özellikleri ile yara pansumanında kullanılmaktadır.
- Bakır, Cu etkileri; hücre içi oksidasyon sürecini katalize edebilir ve virüs ve bakterileri inhibe edebilir ve yara tedavisi için iyi antibakteriyel ve antiviral etkiler gösterir. Normal insan serumunda Cu 2+ 'nın ortalama konsantrasyonu 0,94 ± 0,11 mg/L olarak bildirilmiştir. Yara iyileşmesinde dokuda Cu 2+ konsantrasyonları araştırılmış, yaranın iyileşem sürecinde ilk 7 günde önemli bir değişiklik gözlenmezken, sonrasında kademeli olarak artmakta 21 gün sonra 1,24 ± 0,25 mg/L'ye ulaşmakta ve 42 gün sonra normal seviyelere dönmektedir. Cu 2+ çeşitli enzimlerin aktivitesini etkileyebilir, nükleik asit metabolizmasını ve protein sentezini destekleyebilir, kolajen lifleri ve kolajen sentezini indükleyebilir. Bunların hepsi yara tedavisi için oldukça önemlidir. Dahası, Cu 2+, Ag +'ya benzer bir antibakteriyel etki gösterir. Klinik olarak, artırılmış Cu 2+ aktivitesi yaralarda kılcal damar oluşumunu uyarabilir ve Cu 2+ içeren yara pansumanları yara iyileşmesini destekleyebilir. Cu 2+ ve glisin-histidin-lizin (GHK) kombinasyonuyla oluşan bakır peptid, serumdan izole edilen, elastin ve kolajen sentezini destekleyen, kan damarı büyümesini artıran, antioksidan kapasiteyi iyileştiren ve ciltte glikoz-poliamin üretimini uyararak cilt çoğalmasını ve kendi kendini onarmasını destekleyen bir bakır kompleksidir. Sonuç olarak, Cu 2+'nin yara iyileşme sürecinde iki ana işlevi vardır. 1) Cilt üzerinde koruyucu bir etki uygular ve cilde oksidatif hasarı önler ve 2) Cildin rekombinasyon sürecini tetikler ve hasarlı cildin uzaklaştırılmasını ve normal cildin yenilenmesini başlatır.
- Demir, Fe 2+ /Fe 3+ etkileri; Fe'nin derideki fizyolojik rolü karmaşıktır, seviyeleri sabit değildir ve yaşlanma sürecinde artar. Fe epidermiste birikir ve konsantrasyonu dış tabakadan içe doğru artar, epidermisin bazal tabakasında en yüksek konsantrasyon 7.33 ± 0.98 µmol/g'a ulaşır. Fe iyonlarının homeostazı, transkripsiyon faktörlerinin, Fe düzenleyici ve depolama proteinlerinin ifadesine ve aktivitesine bağlıdır. Kronik yaralarda Fe içeriği akut yaralardan daha yüksektir. Kronik yaraların iyileşmesinin zor olmasının nedeni, kronik hastalığın neden olduğu anemi ve lokal kutanöz demir hemostazının düzensizliği ile ilgili olabilir. Fe yara yüzeyinde çeşitli etkiler yol açmaktadır;
- Fe doku oksijen içeriğini etkileyebilir. Fe eksikliği demir eksikliği anemisine yol açar ve sonuçta doku hipoksisine neden olur. Demir eksikliği anemisinin neden olduğu doku hipoksisi fibroblast bölünmesini, kollajen üretimini ve yeni kan damarı büyümesini engelleyebilir ve böylece doğrudan yara iyileşmesini etkileyebilir.
- Fe kollajen sentezini etkileyebilir. Fe eksikliği kollajen sentezinde zararlı etkilere neden olur. Kollajen büyüyen hücrelere bağlanır ve kollajen sentezinin tıkanması yara iyileşmesini olumsuz etkiler.
- Fe ayrıca oksidatif stres seviyelerini de etkileyebilir. Ortamda serbest Fe aşırı olduğunda, yara iyileşmesinde önemli bir rol oynayan oksidatif stresi indükleyerek REDOX homeostazını bozabilir. Fe esas olarak Fe 2+ (elektron donörü) ve Fe 3+ (elektron alıcısı) formunda stabil olarak bulunur ve yara iyileşmesinin tüm aşamalarını etkileyebilir.
- Fe aşırı yüklenmesi makrofajların aktivasyonunu etkiler. Fenton reaksiyonu tarafından indüklenen ROS ve kalıcı M1 makrofajları tarafından salgılanan proinflamatuar sitokinler yaralarda yüksek oksidatif stres ve inflamasyon durumuna neden olur.
- Fe aşırı yüklenmesi fibroblast yaşlanmasına yol açar. Demir aşırı yüklenmesinin neden olduğu oksidatif stres, fibroblast yaşlanmasının başlıca nedenidir ve lizozomal fonksiyonların bozulması, demir depolama proteinlerinde artış ve demir ölüm duyarlılığında azalma ile ilişkilidir. Dahası, yaşlı fibroblastların kalıcılığı kronik cilt yara iyileşmesinin normal ilerlemesini engeller.
Fe-şelatlayıcı ajanlar veya Fe içeren farmakolojik ilaçlar bu nedenle kronik yaraların tedavisinde kulanılmaktadır.
- Çinko, Zn 2+ etkileri; Zn içeriği normal yetişkinlerde yaklaşık 1,4-2,4 g'dır ve cilt dokusunun sağlığını koruyabilir ve bağışıklık fonksiyonlarını iyileştirebilir. Cilt dokusu hasar gördüğünde ve bir yara yüzeyi belirdiğinde, Zn içeriği değişir. Yanık yaralarında, cilt dokusundaki Zn 2+ içeriği 1-3. günlerde azalır ve 7. günde artar. Yara iyileşmesi ve iltihaplanma sırasında büyük miktarlarda Zn 2+ tüketilir. Bu nedenle oral veya lokal topikal Zn kullanımı yara iyileşmesini desteklemek için kullanılabilir. Dahası, Zn kılcal damarlarda, granülasyon dokusunda ve fibroblastlarda artışı destekleyebilir ve yanıklar, cerrahi yaralar, alt ekstremite ülserleri, yatak yaraları ve cilt iltihabı gibi çeşitli yaraların iyileşmesini etkili bir şekilde destekleyebilir. Ek olarak, Zn doku onarımında rol oynayan önemli bir koenzimdir ve birçok proteinin bir bileşenidir. Ayrıca pıhtılaşmada, hücresel bağışıklık düzenlemesinde, epitel rejenerasyonunda ve hücre dışı matris birikiminde önemli bir rol oynar. Zn 2+ hücre çoğalmasının ve farklılaşmasının düzenlenmesine veya bakteriyel hücre zarı yapılarının korunmasına katılabilir, epidermal hücre çoğalmasını uyarabilir, fibroblastlar tarafından kolajen birikimini destekleyebilir, inflamatuar faktörleri inhibe edebilir, hücre çoğalmasını ve göçünü destekleyebilir, granülasyon dokusu oluşumunu ve anjiyogenezisi destekleyebilir ve ciltteki inflamatuar yanıtı düzenleyerek yara yüzeyinin epitelizasyon sürecini hızlandırabilir.
Çok sayıda klinik çalışma, yaralarda Zn içeren tıbbi pansumanların kullanılmasının iyileşme süresini kısaltabileceğini göstermiştir. Yara tedavisi bağlamında, Zn pansumanlarda öncelikle çinko oksit (ZnO) veya çinko sülfat (ZnSO4) formunda bulunur; burada, ZnO parçacıkları suda çözünmez ve proteinler içeren sulu bir çözeltide çözülür. Bu nedenle, Zn 2+ yaraya sürekli ve yavaş bir şekilde salınabilir, ancak ZnSO4 yavaş salınım etkisi göstermez.
Magnezyum, Mg2+ etkileri; Mg 2+ hücrelerde en bol bulunan katyonlardır ve yumuşak dokularla yakından ilişkilidir. Mg 2+ konsantrasyonu, insan deri fibroblastlarının göçünü ve yapışmasını doza bağlı bir şekilde etkiler; 100 μmol/L ve 1 mmol/L MgCl2 çözeltileri fibroblastların göçünü önemli ölçüde destekleyebilir. Mg 2+, 100 μmol/L'lik bir tepe konsantrasyonunda insan göbek kordonu endotel hücrelerinin göçünü düzenleyebilir ve ayrıca anjiyogenezi destekler. Mg 2+, olgun yara dokusunun rejenerasyonu için gerekli olan kolajen sentezini destekler.

