- Gösterim: 9586
Otoimmünitenin(immun sistemin kendi dokularına saldırması, kendi antijenlerine karşı antikor geliştirmesi) vücudumuzda düşündüğümüzden daha sık gerçekleştiğini ancak bunun sonucu olması gereken otoimmun hastalıkların nadir geliştiğini biliyoruz(50 yaş üzerindeki kadınların % 50 sinden fazlasında antinüklear antikor-ANA pozitif olmasına rağmen otoimmun hastalıkların % 2 den az görülmesi sonucunda olduğu gibi). Vücudun otoimmun hastalıklara karşı ek güvenlik seviyeleri ile korunduğu düşünülmekte. Ayrıca otoimmun hastalıkların bir grubunda klinik davranışına bakıldığında klinik tablonun sürekli olumsuz tablo ile seyretmediği, hastalığın kısa klinik alevlenme dönemleri ve uzun durgunluk dönemleri(halen otoantikorlar olmasına rağmen) ile seyrettiği görülmekte bunun nedenleri olarak yine bu güvenlik tedbirleri gösterilmekte.
Deri olağanüstü yapısı ile en aktif bağışıklık organımız. İmmun yapısı ile çevresel patojen mikroorganizmalara karşı antimikrobiyal peptitler, kimyasallara karşı ligandlar(örneğin, aril hidrokarbon reseptör ligandları gibi) ve çevresel fiziksel ve mekanik strese karşı kemokinler, sitokinler, proteazlar üretmekte. Bu sayede deri(özellikle epidermis) dış etkenlere karşı bariyer fonksiyonunu düzenlerken genel bağışıklık sistemini etkilemekte/etkilenmekte.
Derinin inflamatuar hastalıklarının klinik çeşitliliği(sedef hastalığının; guttate, plak, ters, seboreik ve eritrodermik, lokalize ve generalize formları ve püstüler klinik formlar gibi) immun cevabın ortaya çıkışında TNF, IL-23/IL-17, IL-22, IL-4/IL-13, TGF-b ve IFN-g gibi birçok farklı sitokin ve kemokin aracının rol oynamasından kaynaklanmakta( sitokin ve kemokinlerin tek başlarına yanıtları farklı klinik ve histolojik özellikler göstermekte). Bu karşın bazı inflamatuar deri hastalıkları, atopik dermatit gibi, kliniği nerede ise stadartdır ve çeşitlilik göstermemektedir.
İnflamatuar deri hastalıkları sınırlı klinik, serolojik ve histolojik bilgilerimize ve bulgularımıza rağmen son yıllarda 4 ana gruba ayrılmakta(immun cevabın parternine göre);
1. Likenoid patern; dermatitis ve epidermal deri hücreleri olan keratinositlerde apoptosis
2. Ekzamatöz ve blistering(su toplamları) patern; lezyonlarda egzama, akantozis ve epidermolizis görülmekte
3. Psoriatrik patern; epidermal akantozis ile kalınlaşma, ve epidermise nötrofillerin geçişi, ekzositozu.
4. Dermal patern; epidermisten çok dermiste fibrotik(musin ve kolajen birikimi) ve granulomatöz(dermiste granulomlar) değişimler gözlenmekte.
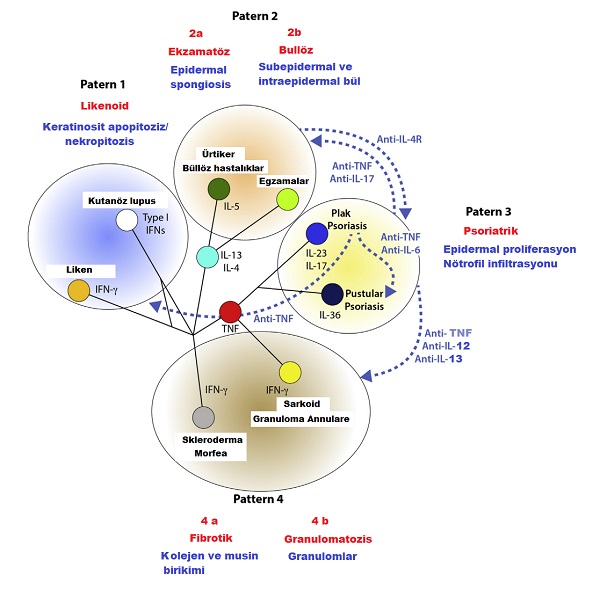
Her paternde inflamatuar mediyatörler rol oynarken bazı sitokin ve kemokinlerin dominant oldukları görülmekte. Örneğin likenoid paternde IFN-γ, ekzamatöz ve blistering paternde IL-4 ve IL-13, psoriatrik paternde IL-17 ve dermal paternin fibrozisite TGF-β gibi. Aynı hastalığın farklı klinik fromlarında farklı immünolojik yanıt paternleri ile kliniğin değişimi(örneğin guttat sedef hastalığından plak sedef hastalığı veya plak sedef hastalığından jeneralize püstüler sedef hastalığı) yada immunolojik yanıtın kaybolması ile kliniğin zaman zaman azalması-kaybolması paradoksal reaksiyonlar görülmekte. Farklı klinik paternlerin belirlenmesi tedavinin seçimindede önemlidir. Ancak aynı tanıya sahip hastalarda paterne göre seçilen ilacın yanıtlarında farklılıklar hatta tedavi başarısızlıkları görülmekte. Bunlar hastaya özgü serum ilaç düzeyleri ve metabolizmadaki farklılıklar ile açıklanmakta. Ayrıca tedavide kulanılan bazı ilaçların paradoksal başka deri problemlerine yol açması bu mekanizmalar ile açıklanmakta(psorisiste kullanılan TNF inhibitörleri ilaçlarının egzama, palmoplantar pustulosis, liken planopilaris, sarkoidozis, pyoderma gangrenosum yapması paradoksu gibi). Bu sonuçlar deri immunitesi ve otoimmun hastalıklarda bilgilerimizin halen yetersiz kaldığı durumlar.
Derinin otoimmun hastalıklarının klinik tanısında; deri ve/veya mukozanın tutulumuna, klinik bulguların özellikleri ve davranışına, deri otoimmun hastalıkları ile sistemik organların tutulumların birlikteliklerine(dermatit herpetiformis ilişkili çölyak hastalığı, pemfigus-pemfigoid-ilaç aşırı duyarlılığında zeminde sistemik bir malignite riski gibi), altında yatan diğer spesifik otoantikorların laboratuvarda araştırılması,... gibi özelliklere bakılmakta.
Otoimmun hastalığın tanısında ve aktivitesinin takibinde spesifik otoantikorların deride hedeflerinin yani derideki antijen yapılarının bilinmesi önemli. Deride otoantikor-antijen ilişkisini biraz hatırlayabiliriz.
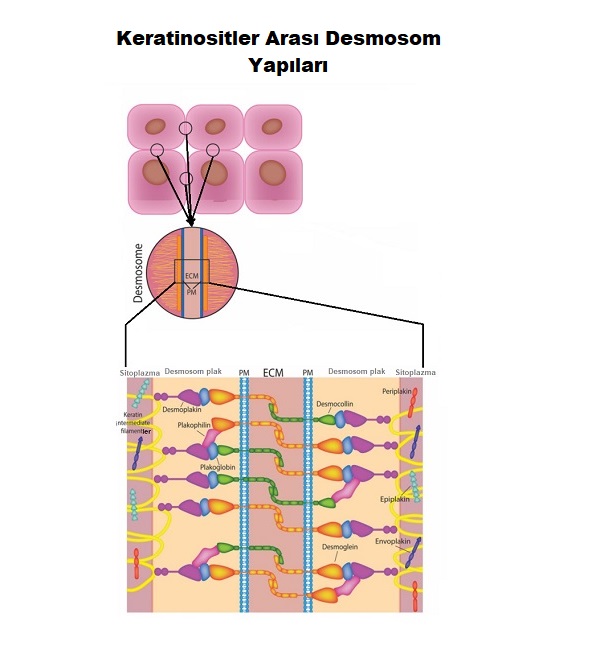
Epidermal hücreler olan keratinositlerin birbiri arasındaki yapısal bağlar desmosome olarak tanımlanır. Desmosomlar hücre içi ve hücreler arası birçok proteinden oluşan bir komples yapıdır ve keratinositleri birbirine sıkıca bağlamakta. Epidermisin mekanik direncini ve bütünlüğünü sağlamakta. Desmosomlar ayrıca hücre çoğalması, farklılaşması ve morfogenez gibi temel süreçlere katkıda sağlamakta. Otoimmun deri hastalıklarının bazılarında otoantikorlar bu desmosom kompleksine karşı gelişmekte. Bunların bozulması hücreler arası bu kompakt yapının gevşemesi ve parçalanması ile sonuçlanmakta. Otoantikorlar desmosomal kompleksi oluşturan başlıca "desmoglein ve desmocollin" proteinlere karşı oluşmakta.
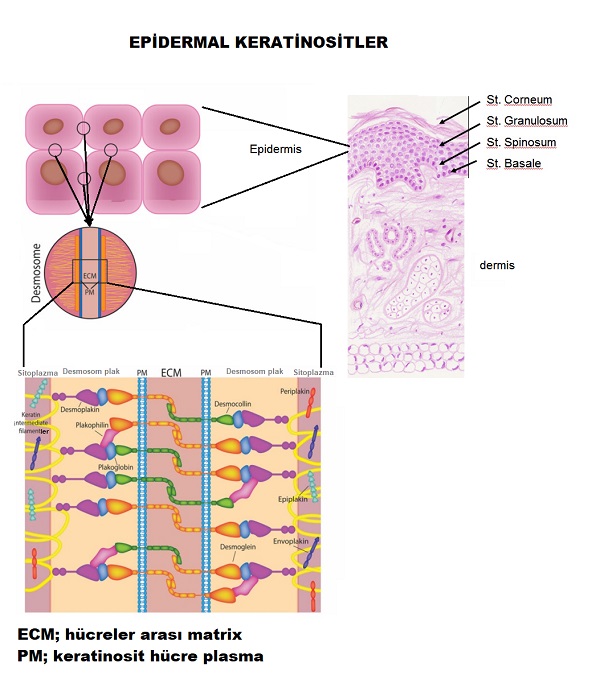
Otoimmun hastalıklar dışında;
- bullöz impetigo ve stafilokok kaynaklı scalded skin sendromlarda (bakteriyal kaynaklı eksfoliatif toksinler) desmoglein 1 karşı antikorlar gelişebilmekte,
- adenovirus enfeksiyonlarında desmoglein 2 karşı antikorlar gelişerek idrar ve solunum yollarında epitelin bütünlüğü bozulabilmekte,
- genetik desmosomal hastaıklarda deride saç kayıpları ile kalp hastalıklarının birliklte olması
- bazı tümörlerde tümörün büyüme aşamasında desmosomal proteinlerin aşırı yapımnın artması görülmekte.
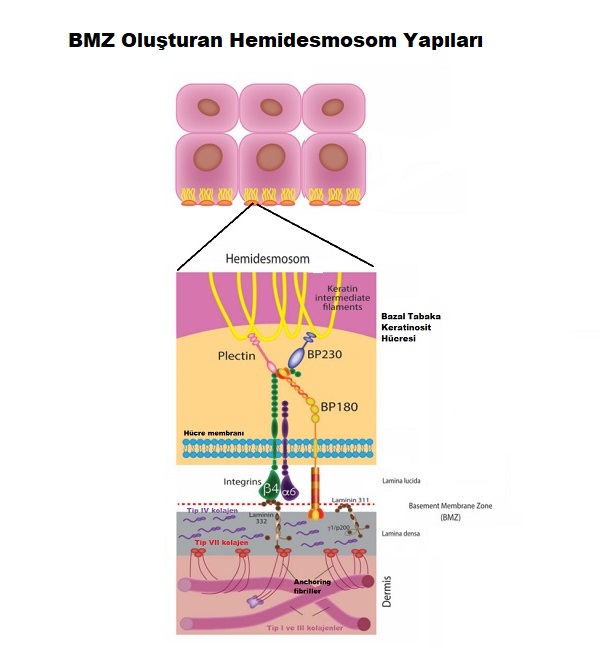
Epidermisin dermise sıkı tutunmasını sağlayan, epidermal basal membranında birçok protein kompleksleri bulunmakta ve bunlar hemidesmosome olarak tanımlanmakta. Hemidesmosome yapıları deride, korneada, sindirim solunum sisteminin bir kısmında ve amniyotik epitelde bulunmakta. Yapısal görevleri dışında hemidesmosomlar hücre çoğalması, farklılaşması ve hücre ölümünün temel süreçlerinde katkı sağlamakta. Derinin otoimmun hastalıklarda otoantikorlar bazal mebran zonundaki hemodesmozomları oluşturan protein komplekslerine karşı gelişmekte. Örneğin hemidesmosom protein komplesinden olan BP180 "bullous pemphigoid antijen 2 - BPAg2 olarakta bilinmekte. BP 180 bazal tabaka keratinosit hücre içerisinden başlayarak bazal tabaka zonunda lamina densaya kadar uzanmakta. BP180 nin hüre dışı kısmı NC16A olarak tanımlanır. NC16 A bullous pemphigoid ve pemphigoid gestationis bülloz hastalıklarında otoantikorların en yoğun bağlandıkları alan. NC 16 A karşı gelişen IgG yapısında otoantikorlar bu hastaların serumlarında ELISA yöntemleri %80 - 90 oranında pozitif olarak saptanmakta. Aşağıdaki temsli resimde BP 180 yapısında tanımlanan C-terminaline karşı otoantikorlar mukozal tutulumlun hastalıklarda görülmekte. Linear IgA birİkimine bağlı gelişen büllöz hastalıklarda ise BP180 nin LAD-1 ve LABD97 bölümlerinin antijen olarak algılandığı görülmekte.
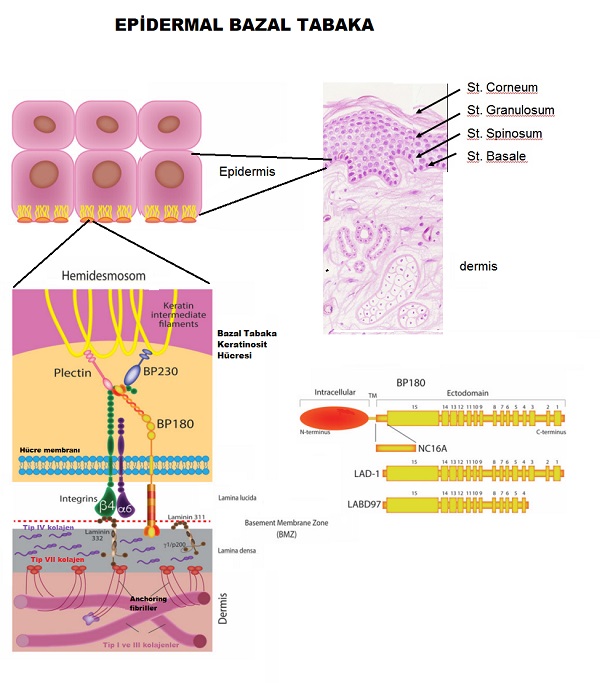
Otoimmün dermatolojik hastalıkların tanısında;
- hastalıklı yada sağlam deri doku örneklerinde otoantikorların direkt immünofloresan-DIF
- hasta serumunda otoantikorlar indrekt immünofloresan-IIF ve
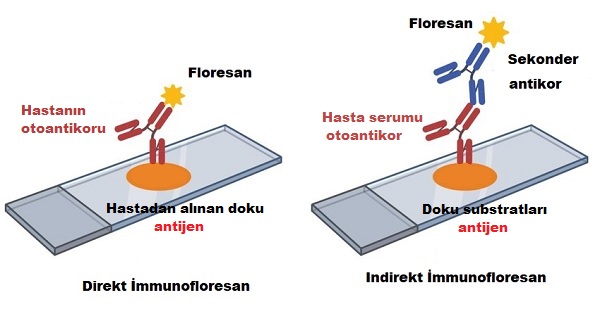
- hasta serumunda "Western blotting- immunoblotting ve immunoprecipitation gibi yöntemler kulanılarak spesfikik otoantikorlar saptanabilir. Ancak bu testler daha özel ve uzmanlık gerektiren laboratuvarlarda yapılabilmekte. ELISA testleri daha anlamlıdır. ELISA eğer IIF ve DIF ile komkbine kullanıldığında dermatolojik otoimmun hastalıkların tansıında daha spesifik ve duyarlı yöntemler olmakta.
Klasik patolojik değerlendirmelerde hastalıklı deri ve mukoza örnekleri alındıktan sonra formol ile fikse edilmekte. Ancak bu şekilde fiksasyon örnekleri DIF testleri için kullanılamaz. Formole maruz kalan biyopsi örnekleri 2-10 dakika sürelerde immünoreaktan özelliklerini kaybetmeye başlar. Bu nedenle DIF doku örnekleri serum fizyolojik içerisinde ve taze olmalıdır.
Deri otoimmun hastalıklarının tanısında DIF altın standart olarak önemli. Ancak DIF yapılamıyor ise IFF çalışılmalı. IIF, dokuda immunofloresan boyanma modeline ve antikor formuna dayalı olarak çeşitli immünobüllöz hastalıkları sınıflandırarak tanıda önemli bir rol oynar.
IIF doku immunofloresan boyanma modelleri; bu modeller ve antikor grupları(IgG ve ıg A gibi) tanı dışında tedavi seçimindede belirleyici olmakta.
- epidermal hücre yüzey antijenlerine karşı otoantikorlardan kaynaklanan immunofloresans boyanma modeli; cell surface-CS olarak tanımlanır ve tipik olarak pemphigusta görülür. Buradaki antikorların alt grupları hastalıklara göre Ig G, IgG4 ve Ig A dan oluşmakta.
- epidermal bazal membran yüzeyindeki antijenlere karşı otoantikorlardan kaynaklanan immunofloresans boyanma modeli; basal mebran zone-BMZ olarak tanımlanır ve tipik olarak pemfigoidde görülmekte. 3 alt formu bulunmakta;
- oluşan bülün tavanında-epidermal BMZ floresan boyanma
- bülün tabanında-dermal BMZ floresan boyanma ve
- kombine boyanma
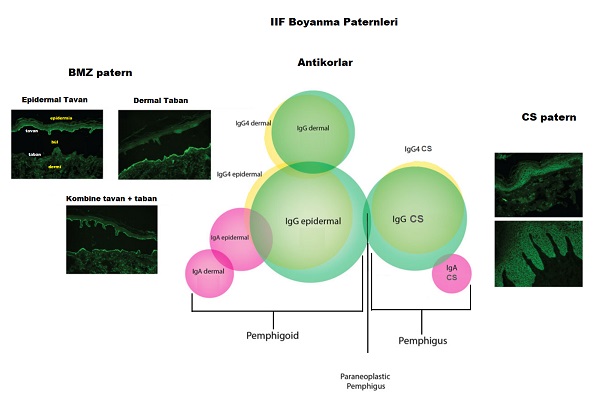
Hasta serumunda ELISA gibi yöntemler ile saptanabilen spesifik antikorlar epidermal hücre yüzey antijenlerine; cell surface-CS antijenleri ve bazal membran BMZ antijenlerine karşı oluşmakta. ELISA testleri hastalığın aktivasyonunun ve tedaviye cevabının değerlendirilmesinde de kullanılmakta. Örneğin pemfigoidde IgG BP180 antikor değişimlerine ve pemfigusta IgG desmoglein antikor seviyelerinde değişimlere bakılabilir. Bazı otoimmun deri hastalıkları için spesifik ELISA antijenleri henüz belirlenmemiş(linear IgA hastalığı gibi). ELİSA yöntemi ile otoantikorların IgG ve A gibi guruplarına bakılabildiği gibi alt gruplarıda değerlendirilmekte. Örneğin büllöz otoimmün hastalıklarda IgG4 ön plana çıkmakta.
- BMZ antijenleri
- BP180 -BP230 (bullous pemphigoid spesifik)
- tip VII kolajen(epidermolysis bullosa acquisita-EBA ve bullous lupus erythematosus spesifik)
- epidermal hücre yüzey antijenleri
- desmogleins 1 (pemphigus foliaceus için spesifik)
- desmogleins 3( pemphigus vulgaris için spesifik)
IIF ve ELISA serum testi ile birlikte DIF doku testi, otoimmun deri hastalıklarının tanı, takip ve kontrollerinde oldukça hassas ve önemli tanı araçlarıdır.
Otoimmun deri hastalıklarını klinik, otoantikor-antijenik yapı, duyarlı-spesifik testler gibi özelliklerine göre gruplar halinde değerlendirebiliriz.
Klinikte Büller ile Karekterize Otoimmun Deri Hastalıkları
Bunlar büllöz deri hastalıkları olarak bilinmekte. Otoimmun hastalıklar ve tanı yöntemleri hakkında bilgilerimizin yeterli olmadı dönemlerde bu hastalıklar tanımlandığı için maalesef bu gruptaki hastalıkların sınıflması ve verilen isimler birbirleri ile çok karışmakta. Pemfigus ve pemfigod hastalıkların isimsel benzerlikleri gibi. Son yıllarda büllöz otoimmun hastalıklarda otoantikorların klinik ve epidermal antijen hedefine göre basit bir gruplandırma yapılmıştır.
- gergin bül yapısına sahip büllöz deri hastalıklar; yapısal özelliklerini kolaylıkla kaybetmeyen ve gergin büllerin var olduğu bu grupta otoantikorların hedefi BMZ yani BMZ nun antijenik yapılarıdır.
- gergin olmayan gevşek bül yapısına sahip büllöz deri hastalıklar; yapısal özelliklerini hemen kaybeden ve gevşek büllerin var olduğu bu grupta otoantikorların hedefin keratinosit hücre yüzeyleri-CS yani CS antijenik yapılardır.
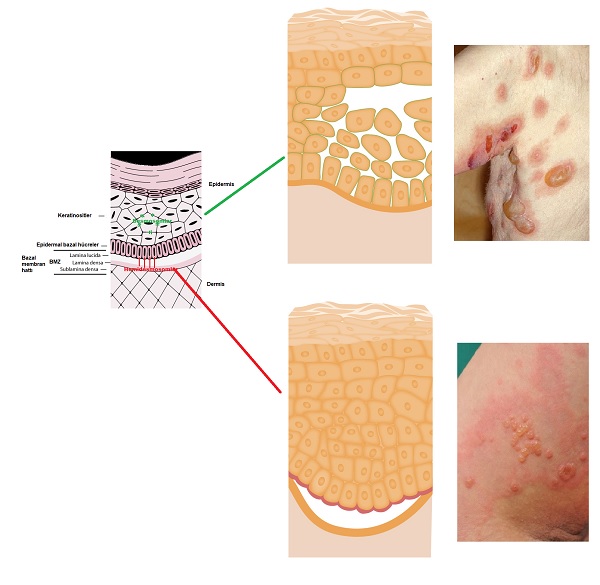
BMZ antikorları ile birlikte olan otoimmun deri hastalıkları
Bu hastalıklarda BMZ oluşturan hemidesmosomal ve diğer birleştirci moleküllere karşı antikorları geliştiği görülmekte. Bu otoantikorlar epidermal BMZ de inflamasyon ve yapısal bozulmalara neden olarak epiderrmisin dermisten ayrılmasını sağlamakta. Klinik olarak gergin bül yapısı ve/veya bül çevresinde inflamasyon kaynaklı ürtikerya yada egzamatöz lezyonlar görülmekte. Sıklıkla mukozal tutulumlarda görülmekte(köbnerizasyon pozitif olduğu için daha çok travmatik mukozal alanlarda).
Pemfigoid-Pemphigoid
Bu grupta "Bullous Pemphigoid (BP) ve Mukozal Membranların Tutulduğu Pemphigoid (MMP)" yer almakta.
BP en sık görülen büllöz otoimmun hastalıklardan. Sıklıkla ileri yaşlarda görülmekte. Klinikte büller dışında en belirgin klinik bulgu lezyonlarda büller öncesi/sırasında/sonrasında kaşıntının varlığıdır. Hatta bül olmadan sadece kaşıntı bile görülebilmekte.Büller vücudun her alanında çıkabilmekle birlikte sıklıkla koltuk altı ve kasık gibi katlantı yerlerlerini tercih etmekte. MMP ise sadeec mukozal büller görülmekte. BP nin iyileşme sürecinde deride sekel kalmaz iken MMP de mukozal iyileşmede sekel kalabilmekte. Pemfigoid klinğinde büller gergin ve sıklıkla kolay bozulmadıkları için klinik muayenede rahatlıkla görülebilmekte. Büllerin ürtikeryal bir zeminde görülmesi çok tipiktir. BP klinik alt grupları; yenidoğan/çocuk BP, lokalize BP(bacaklarda sıklıkla görülmekte), eritrodermik BP, vulvar BP, vejetatif BP(koltuk altı ve genital alan yerleşimli), dishidrıtik form BP(el içi ve ayak tabanında), nodular BP gibi.
MMP klinik alt grupları; cicatricial pemphigoid, göz tutulumu gösteren ocular cicatricial pemphigoid, Brunsting–Perry pemphigoid, Anti-laminin-332 pemphigoid gibi. Mukozal büller sıklıkla klinik muayenede görülemez, bunlar yerine bunların yırtılması ile erozyonları ve sonrasında gelişen skar sekellleri görülmekte. Antilaminin-332 pemphigoidin % 30 oranlarda altta yatan bir maligniteye bağlı olarak geliştiği untulmamalıdır. Brunsting–Perry formunda ise muozada büller skarsız iyileşirken baş ve boyunda skarlar ile iyileşen büller klinik olarak görülmekte.
- DIF; BP ve MMP ile pemphigoidin tüm varyantlarında DIF testinde BMZ de tırtıklı görünümde çizgisel olarak lgG ve/veya C3 birikimi saptanmakta. DIF de tırtıklı çizgisel boyanmanın paterni yani n yada u harfi şeklinde olmasıda son derece önemlidir. DIF de n harfi gibi(aşağıdaki gibi) ve bülün tavanında ise bu BP ve MMP tanısını destekler iken DIF de u harfi gibi ve bülün tabanında ise EBA ve büllöz Lupusu destekler(tip VII kolajen otoantikorları). DIF testi BP ve MMP için tanısal açıdan altın standart.
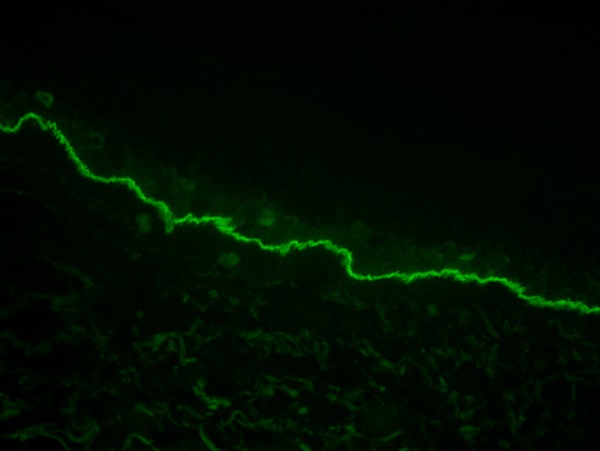
- IIF; hasta serumunda IIF çalışmaları yapılarak BMZ karşı otoantikorlar gösterilebilir. DIF yapılamıyor ise ve pemphigoidlerin alt klinik formlarının ayrıcı tanısı düşünülüyor ise IIF yapılması düşünülmelidir.
- BP de hasta serumu + split edilmiş(sıklıkla tuzlu ortamda BMZ dan epidermis ile dermisin ayrıldığı kadavra yada cerrahi olarak çıkarılmış deri örnekleri) hastaya ait olmayan deri örneklerinde IIF testi yapıldığında IgG otoantikorların bu split derinin tavanında-epidermal tarafında yada epidermal-dermal(tavan + taban) kombinasyonunda biriktiği görülmekte. MMP de yarıda fazla hasta gurubunda IIF testi negatif sonuçlanmakta. MMP de IIF nin pozitif olduğu olgularda ise IgG otoantikorların bu split derinin tavanında-epidermal tarafında biriktiği görülmekte.
- IIF floresan boyanma split edilmiş derinin üst tavanında olmakta. Buda otoantikorların BMZ nin epidermal tarafına karşı; lamina lucida ve üstüne karşı geliştiğini ifade etmekte. Otoantikorlar bu alandaki BP180, BP230, integrin 6α ve integrin 4β proteinlerine karşı gelişmekte.
- IIF de hasta serumu + split edilmiş deride splitin alt tabanında immunfloresan boyanma otoantikorların BMZ nin dermal tarafına karşı geliştiğini ifade etmekte. Bu formda IIF EBA ve bullous LE tanısında anlamlıdır. Ayrıca bu floresan boyanma pemphigoidlerde görülürken tip VII kolajen(anti-p200, laminin gamma-1) ve anti-laminin-332 proteinlerine karşı otoantikorların geliştiğini göstermekte.
- IIF BP de % 76-73 duyarlılık ve %100-96 spesifiklik göstermekte, bu oranlar BP de DIF testlerindeki duyarlıklık ve spesifititesinden bile yüksek. Bu nedenle BP de altın standart IFF olabilir.
- ELISA; hasta serumunda ELISA çalışmaları yapılarak serumda BMZ karşı otoantikorlar gösterilebilir.
- Bullous pemphigoid ELISA testinde 2 antikor; BP180 ve BP230 bakılmakta. BP180 yüksek titreleri BP tanısında % 95-54 oranında duyarlı ve % 99-90 oranlarında spesifiktir. Ancak BP 180 MMP de fazla saptanamaz. BP230 pozitifliği % 82-48 duyarlılık ve % 99-65 oranında spesifite göstermekte. Bu düşük oranlar ile BP tanısında BP 180 kadar tek başına kullanılmaz.
- BP180 antikor titraleri hastalığın aktivitesinin takibinde kullanılmkata.
- BP230; bullous pemphigoid antijen 1 (BPAg1) ve BP180 bullous pemphigoid antijen 2 (BPAg2) olarak bilirnmekte.
- anti-p200 otoantikor pozitifliği pemphigoidin genç yaşlarda ortaya çıkabileceğini göstermekte.
- anti-laminin-332 antikorları pemphigoidin muozal tutulumunu göstermekte
Pemfigodin alt klinik varyantı olan p200 (laminin gamma-1) pemphigoid büller ve kaşıntılı ürtikeryal plaklar BP benzer. Klinik yerleşimi el içi ve ayak tabanı, saçlı deri ve mukozalaradır. Sıklıkla skar ve milia gelişimi ile iyileşmekte. %30 psoriasis ile birlikteliği görülmekte. Burada antijen BMZ de lamina densada p200 (laminin-311 c1 subunit) proteinleri. Bunlarda DIF de BMZ da lamina densada-dermal tarafta floresans birikimi n şeklinde boyanma paternine neden olmakta. Serum ELISA testlerinde IgG tip VII kolajen, IgG BP180 ve IgG BP230 antikorlar gösterlebilir. Serum IgG p200 antikor haen geliştirime aşamasında.
BP de altın standart IFF olabilir.
Pemphigoid Gestationis (PG)
Pemphigoid gestationis gebelik döneminde, kaşıntılı papüller, ürtikeryal plaklar ve büller ile karekterize büllü otoimmun deri hastalıkları içerisinde yer almakta. Gebelikte sıklıkla göbek çevresinde lezyonların başladığı gözlenmekte. Tekrarlayan gebelikler, hormonsal tedaviler ve adet dönemlerinde klinik yeniden ortaya çıkmakta. PG varlığı gebelikte erken doğum ve düşük doğum ağırlıklı bebek risklerine neden olmakta.
- DIF; PG tanısında klinik olarak lezyonun hemen sınırından alınan deri biyopsi örneklerinde DIF de BMZ de hemidesmosomlara karşı çizgisel güçlü C3 birikimi görülürken IgG birikimi yok yada zayıftır. Benzer sonuçlar hasta serumundan yapılan IIF testinde de görülmekte.
- IFF; Serum ile yapılan IIF testlerinde BMZ da deri splintin epidermal(tavan) tarafında IgG + kompleman birikimi gözlenmekte. Bu kompleman fiksasyonu tarihsel olarak adlandırılan, herpes gebelik faktörünü (HGF) olarak tanımlanmakta. Bununla birlikte bu test günümüzde yaygın olarak yapılmaz.
- ELISA; serumda ELISA ile otoantikor testlerinde ise IgG BP180 antikorları artmış(NC16A karşı gelişmiş antikorlar). Serumda ELISA ile ölçülen IgG BP180 antikor seviyesi BP kliniğini değerlendirmek için kullanılırken IgG BP180 antikor seviyesi PG kliniği ile ilişkili değil. PG hastalarının bazı alt gruplarında çöliak hastalığı için karekteristik olan otoantikorlar yüksek bulunabileceği unutulmamalıdır. BP23o karşı antikor gelişimi var ancak nadir.
PG'de neredeyse her zaman artmış olan ELISA'nın IgG BP180 antikor seviyesi ve DIF tanısal belirteç olarak yeterli olabilir.
Epidermolysis Bullosa Acquisita (EBA)
EBA otoimmun büllöz deri hastalıklarının BMZ dermal formu için güzel bir protip oluşturmakta. Sıklıkla travmatik deri yüzeylerinde ve mukozada gergin büller görülmekte. EBA nın 6 adet kinik varyantı bulunmakla birlikte(klasik/mekanik travma ile bül oluşumu, klasik olmayan/mekanik travma ile bül oluşumu yok, mukozal tutulum, Brunsting–Perry tip gibi) hepsinde klinik tablo BP ye benzemekte. EBA da BMZ da tip VII kolajene karşı otoantikorlar gelişmekte. Tip VII kolajen BMZ da epidermisi dermise bağlayan anchoring fiberleri oluşturmakta. Bu kolejen 3 alfa zincirinin sarmal yapısı ve her ucunda NC1 ve NC2 oluşmakta. Otoantikorlar daha çok NC 1 karşı gelişmekte.
- DIF; DIF de BMZ da lamina densada - dermis tarafında otoantikor birikimine bağlı olarak antikor ve kompleman birikimine bağlı u şeklinde floresans boyanma paterni gözlenmekte.
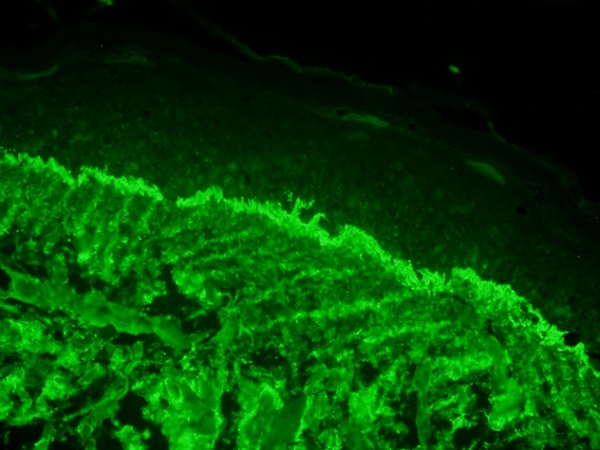
- IFF; hasta serumu ile yapılan IIF testinde split derinin zemininde antikor birikimi ile floresan birikimi görülmekte. FF yüksek duyarlılık ve spesifite göstermekle birlikte Ig G floresan boyanması EBA ve pemfigoidlerde aynı pater gösterdiği için ayrıcı tanıda yeterli değildir. Bu nedenle IFF sonrası ELISA antikolajen 7 bakılması son derece anlamlıdır
- ELISA; hasta serumunda NC 1 ve 2 ye karşı otoantikorlar bakılmakta. ELISA testlerinde anti kolajen 7 antikorlarının gösterilmesi EBA da % 99-86 oranında duyarlılık ve %99-94 oranında spesfiite göstermekte. Kolajen 7 titreleri hastalığın aktivitesinde kullanılabilir. Bu antikorlar büllöz SLE de de görülmekte. Ayrıca kron ve ülseratif kolit gibi hastalıklarda EBA klinik bulguları olsun yada olmasın type VII kolajene karşı antikorlar yükselmekte.
Bullous Lupus Erythematosus (LE)
LE hastalarının 3 de 2 sinden fazlasında tip VII kolajene karşı otoantikorlar görülmekte. LE hastalarında tipik olarak lupus nefrit gibi sistemik tutulumlar ve klasik lupusta görülen anti ds DNA test pozitiflikleri görülmekte.
- DIF; LE tanısı açısından son derece önemli. Bu testte BMZ da granüler yapıda IgG , M ve A antikorlardan oluşan floresans boyanma görülebilir.
- ELISA; LE de 3 farklı klinik from tanımlanmış. Bunlara bağlı farklı otoantikorlar görülmekte.
- tip I LE de en sık otoantikorlar tip VII kolajenin NC1 ve NC2 alanlarına karşı gelişmekte.
- tip II LE de en sık otoantikorlar BMZ nun BP180, BP230, laminin-332 yada laminin-331 proteinlerine karşı gelişmekte.
- tip IIII LE de sık otoantikorlar henüz diğerşeri gibi karekterize edilmemiş.
Linear IgA Hastalığı (LAD)
Klinik olarak pemphigoid ve DH benzeyen derinin otoimmun büllöz hastalıklarından. LAD çocuklarda “chronic bullous disease of childhood” erişkinlerde “linear IgA bullous dermatosis” olarak tanımlanmakta. Her ikisinde de BMZ de IgA birikimi görülmekte. Annuler eritem ve ürtikeryal plaklar üzerinde gergin büller görülmekte. LAD ilaç(en sık vankomisin), enfeksiyonlar, malingniteler, destek doku hastalıkları, inflamatuar bağırsak hastalıkları(özedlikle ülseratif kolit gibi) ile birlikte görülmekte. BMZ hemidesmosomlara ve lamina lucida ve densaya karşı otoantikorlar gelişmekte. Lamina lucidada; LAD-1 (LABD97), BP180 (NC16), BP230 iken lamina densada tip VII kolajene karşı.
- DIF; DIF testi ile BMZ de IgA birikimi gösterilebilir. Birikim lamina lucida ise n patern epidermis boyunca, densada ise U patern dermis boyunca floresans boyanma görülmekte.
- IFF; IFF ile hasta serumu + split deride BMZ da lamina lucida-epidermal(olguların % 91 inde) ve densada-dermal(olguların % 9 unda) IgA birikimi gösterilebilir.
Diğer hastalıklar
Otoantikorların rol oynamadığı derinin bazı büllü hastalıklarında BMZ de DIF bulguları gözlenebilir. Porphyria cutanea tarda ve yalancı profiriada EBA, büllöz LE ve LAD gibi BMZ de DIF bulguları gözlenir. hatta dermiste vaskülit bulgularını destekler DIF birikimleri gözlenebilir(özellikle güneş gören deri örneklerinde).
Keratinosit yüzey-CS antikorları ile birlikte olan otoimmun deri hastalıkları
Keratinosit yüzey antijenleri keratinositleri bir arada tutan desmosom yapıardır. Bu antijenlere karşı gelişen otoantikorlar ile bu süreçte gelişen inflamasyon ile keratinositler arasında desmosomlar ile sağlanan sıkı ilişki bozulmakta büller gelişmekte. Bu akantolizis olarak tanımlanmakta.
Pemphigus
Nadir görülen pamfigus deri ve mukozada desmosom yapısını oluşturan desmoglein ve desmocollin proteinlerine karşı otoantikorların oluşması gelişen otoimmun büllüz deri hastalıkları içerisinde tanımlanmakta. Kliniğinde gelişen büller BMZ büllerinden farklı olarak daha gevşek, kolay bozulur özeliktedir. Bu nedenle klinik olarak deri ve mukozada büllerden daha çok bunların açılmasından kaynaklanan ağrılı erozyonlar görülmekte. Tedavi uygulanmadığında ilerleyici ve yaşamı tehdit edici özelliktedir. Klinik varyantları bulunmakta(pemfigus vulgaris-PV, pemfigus foliaseus...). Bu farklılık desmosomal farklı otoantikorlara göre değişmekte.
Pemfigusun tanısında ve klinik takibinde dokuda DIF testi ve serumda IIF ve ELISA testleri son derece anlamlıdır.
- DIF; Epidermiste desmosomlara karşı Ig G ve C3 birikime bağlı olarak bal peteği
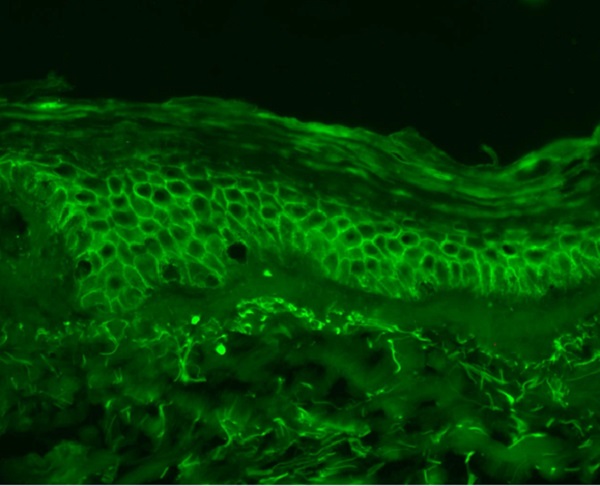
yada noktasal floresan boyanması gözlenmekte.
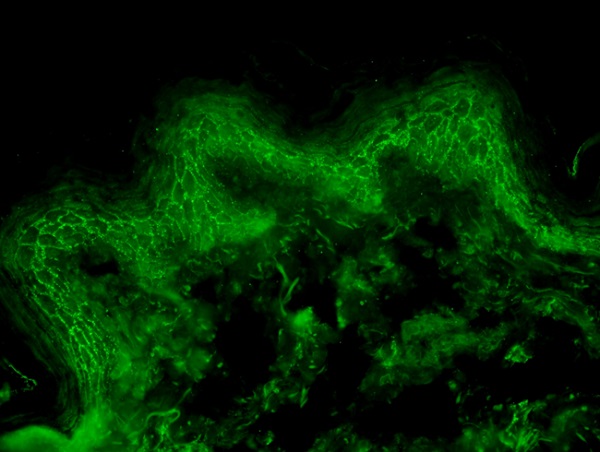
- IFF; Benzer boyanma paterni hasta serumu ile yapılan IFF de de görülmekte. Hasta serum titreleri ile IFF boyamasındaki değişimler hastalığın aktivasyonun değerlendirilmesinde kullanılabilir.
- ELISA; hasta serumunda ELISA testleri ile IgG desmoglein 1 ve IgG desmoglein 3 otoantikorları saptanabilir. IgG desmoglein otoantikorları hastaığın aktivitesi ile korelasyon göstermekte. ELISA testleri ile desmoglein 1 antikorları PV ve foliaseusta saptanabilirken, desmoglein 3 PV saptanabilmekte. Desmoglein 1 pemfigus foliaseus için %98-92 duyarlı ve %100-98 spesifiktir. ELISA Desmoglein 1 ve 3 IIF den daha duyarlı ve spesifik tetsler olarak görülmekte. Ancak DIF % 100-94 oranlarda dıuarlılık ile altın standart. ELISA desmoglein 1 titreleri hastalığın aktivitesinde kullanılabilmekte.
Pemfigus vulgariste-PV; deride inflmasyon olmaksızın gergin olmayan, çoğu zaman yapıları bozulmuş, erode olmuş yada üzeri kabuklanmış büller gelişmekte. Lezyonlarda Nikolskiy ve Asboe–Hansen belirtileri pozitif(Asboe-Hansen belirtisi; sağlam bir bül üzerine basınç uygulandığında bülün sınırıda normal deriye doğru genişlemesi, "dolaylı Nikolskiy işareti" veya "Nikolskiy II işareti" olarak anılır. Nikolskiy belirtisi ise normal deriye yüzeysel yan kaydırma basıncı uygulandığında bül gibi hareket etmesidir.). Mukozal tutulumu belirgin olan PV ve mukoza-deri tutlumu olan olmak üzere klinik varyantları bulunmakta. Sıklıkla ağız içi mukoza, saçlı deri, gövde ve koltuk altında lezyonlar görülmekte. Otoantikorlar IgG yapısında ve desmosomlara karşı; desmoglein 3 karşı gelişmekte(özellikle mukozal varyantında). Desmoglein 3 + desmoglein 1 ise mukoza-deri varyantında görülmekte. PV de doku DIF testinde ve serum IIF tetsinde Ig G ve C3 birikime bağlı olarak bal peteği yada noktasal floresan boyanması gözlenmekte. Serum ELISA testinde ise IgG desmoglein 3 otoantikorları yükselmiş.
Pemfigus foliaseus-PF; endemik pemfigus(fogo selvagem) olarakta bilinmekte. Lezyonlar sıklıkla seboreik alanlarda görülmekte. Büller deride çok yüzeysel yerleşimli bu nedenle sıklıkla klinik olarak gözlenmez. Erozyon ve kabuklanmalar klinikte belirgindir. Sıklıkla neden ilaçlar ve kimyasallardır (Brezilya çevresel kaynaklı fogo selvagem klinğinde olduğu gibi). Otoantikorlar IgG yapısında ve desmoglein 1 karşı gelişmekte. Desmoglein 1 epidemiste daha üst katmanlarda yapılmakta. Bu nedenle PF akantolizis epidermisin daha üst tabakalarında gözlenmekte.
Pemphigus vegetans sıklıkla vücudun koltuk altı gibi katlantı yerlerinde vejetatif, püstüller pemfigus plakları görülmekte. IgG yapısında olan otoantikorlar desmoglein 3 karşı gelişmiş.
Pemphigus erythematosus (Senear–Usher sendromu olarak bilinmekte). Pemphigus foliaceus klinik varyantı ve klinik LE çok benzemekte. Yüzeysel erozyonlar, eritem, kabuklanma görülmekte ve sıklıkla yanalar ve eseboreik alan yerleşmekte.
İlaç kaynaklı pemnfigus immunopatolojisi PF benzemekte.
IgA pemfigus; kaşıntılı kolay açılabilen büller, kabuklar ve erozyonlar görülmekte. IgA yapısında otoantikorlar desmocollin 1 karşı gelişmekte.
Pemphigus herpetiformis eritemli, büller, veziküller, püstüller sıklıkla kaşıntılı ve herpes giibi gruplar oluştruacak şekilde dağılmakta. Otoantikorlar desmosoma desmoglein 1 karşı gelişmekte.
Diğer pemfigus varyantlarının immunopatolojik özelikleri henüz belirlenmemiş.
IFF testinde gözlenen patern "pemfigus benzeri patern" olarak tanımlanır. Bu durum yanılarda, enfeksiyonlarda, ilaç reaksiyonlarında, LE , toksik epidermal nekrozda , temas egzamalarında ve MG- myasthenia gravis görülebilmekte.
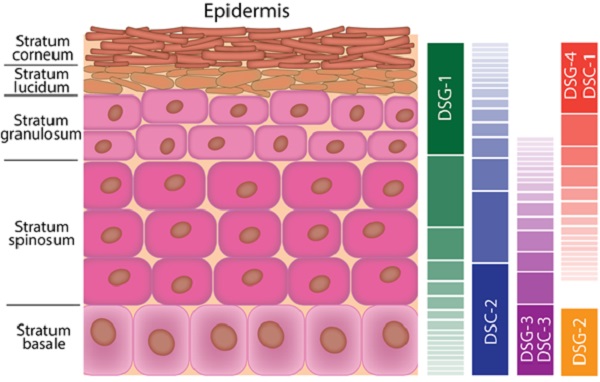
Pemfigusun klinik varyanlatlarının farklılıkları desmosomlarlardaki proteinlerin epidermiste dağılımının farklılığından kaynaklanmakta. Aşağıdaki temsili resimde keratinositler arasındaki bağlantıyı sağlayan ve keratinositler tarafından proteinlerin; "kadtherinlerin-cadherins" epidermal dağlımları renkli barlar ile gösterilmekte. Bunlardan DSG-1; Desmoglein-1 karşı otoantikorlar pemphigus foliaceusta ve DSG-3; Desmoglein-3 karşı otoantikorlar pemphigus vulgariste görülmekte. Bu iki penfigusta klinik özellikler bu desmoglein alt gruplarına bağlı görülmekte. Desmoglein (DSG)-1 ve desmocollin (DSC)-1 çok daha yoğun olarak stratum granulosum ve spinosum yapılmakta ve dermise doğu yoğunluk azalmakta. DSG-3 ise ağız mukoazası eptelinde yoğun olarak yapılmakta, deride ise sadece stratum basaleda yoğun yapılmakta ve stratum spinosuma doğru azalmakta.
DSG-2 ve DSC-2 ise deri epidermis ve epitelin boyunca dada yoğun olarak st. basdalede yapılmakta. Bu ikisdi tüm iç organ epitelillerinde yapılmakta; perikard, plevra, periton, alveol epiteli gibi.
DSG-4 deride başlıca saç folliküllerinden yapılmakta.
BMZ + Keratinosit yüzey-CS antikorları ile birlikte olan otoimmun deri hastalıkları
Bu mikst form her iki immunopatolojik özelliği taşıması ile diğrlerinden ayrılmakta.
Paraneoplastic Pemphigus (PNP)
Vücutta diğer sistemlere ait bir maligniteye bağlı olarak(lenfoma, lösemi, sarkomlar) deride gelişen otoimmun büllöz klinik tablodur. Deri ve mukoza dışında akciğer, sindirim sistemi, böbrekler ve tiroid bezide etklilenmekte. Büller, erozyonlar, ürtikeryal ve likenoid plaklar, eriteme multiforme benzeri plaklar görülmekte. PNP de otoantikorlar desmosomal ve hemidesomosal tüm proteinler karşı gelişmekle birlikte "plakin" proteinlere karşı gelişmekte(plakin proteinler keratinositlerin içerisinde iskelet sistemini oluşturan proteinler).
Deride desmosom ve hemidesmosomlarar karşı otoantikorlar gelişmekte( desmoglein 3, envoplakin, periplakin, desmoplakin 1, desmoplakin 2, BP230, epiplakin, plectin, BP230, desmoglein 1, desmocollin 1, desmocollin 2, desmocollin 3, alpha-2-macroglobulin-like-1 (A2ML1), laminin-332 ve BP180 karşı).
- DIF; DIF te IgG ve Ig A yapısında otoantikorlar BMZ ve CS de floresan boyama yapmakta.
- IFF; PNP IIF testlerinde doku substrartı olarak sıklıkla mesane dokusu kullanılır.
- ELISA hasta serum testlerinde IgG envoplakin otoantikorları PNP için son derece tanısal değeri yüksektir.
Diğer otominnun deri hastalıkları
Dermatitis Herpetiformis (Duhring hastalığı, DH)
Sıklıkla besinler ile gluten alınmasına bağlı olarak deride yoğun kaşıntılı, simetrik yerleşimli, kol - bacak dış kısımlarında(diz ve dirsekler, kalça gibi) lokalize plaklar, veziküller kaşıntıya bağlı ekskoriasyon ile karekterize otoimmun deri hastalığı. Deri belirtileri ile birlikte gluten duyarlılığına bağlı çöliak hastalığı gibi inflamatuar bağırsak hastalığı belirtileride görülmekte. bazen çölika belirtilerin çok önce başlayabilmekte. Burada antijenler keratinositler tarafından yapılan endomysiumda bulunan epidermal transglutaminase-eTG/TG3 dır. Otoantikorların hedefi endomysial otoantikorlaradır(EMA).
- DIF; DIF de subepidermal granuler ve fibriller IgA birikimi görülmekte. Bu birikim normal görünümlü deri örneklerinde %90 oranında görülebilmekte. IgA birikimi dermal damarsal yapılar çevresindede görülmekte.
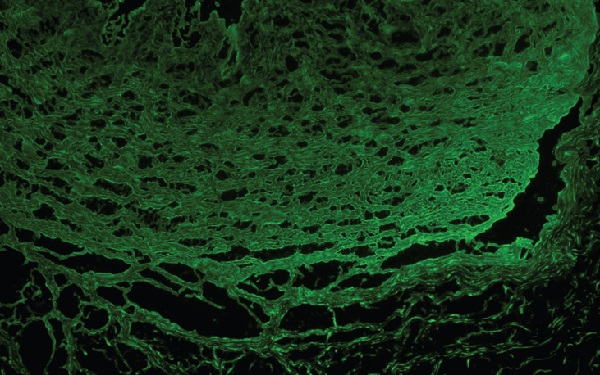
- IFF; DH de IgA otoantikorların epidermal transglutaminase-eTG( transglutaminase 3-TG3 olarakta bilinmekte) karşı gelişmekte. IIF ile IgA yapısında TG3 gösterilebilir. DH lezyonlarında IgA gibi granüler yada agrege pater tarzda fibrinojen birikimi görülmekte. Endomysial antikorlar(EMA) IIF ile gösterilebilmekte. Bunun duyarlılığı % 100-52 ve spasifikliği % 100 dür.
- ELISA; ELISA testleri ile IgA doku transglutaminase-tTG(transglutaminase 2-TG2 olarak bilinmekte) ve IgA eTG/TG3 otoantikorlara bakılabilir.
- DH spesifik doku antijenleri endomysium, eTG/TG3 dir.
- Gliadin otoantkorlarına bakılabilir. Gliadin otoantikorları özellikle spesifik HLA-DQ2 (yaklaşık 95%) yada or HLA-DQ8 (yaklaşık 5%) HLA ti,pelri ile bilriktelik göstermekte.
- ELISA testleri ile IgA tTG/TG2 otoantikorları özellikle çöliak hastalığının tanısı ve hastalığın aktivite takibinde kullanılabilir.
- ELISA IgA eTG/TG3 otoantikorları DH için daha güçlü bir belirteçtir. ELISA Ig A anti doku transglutaminaz (tTG) testlşerin DH % 95-47 duyarlılık ve %100 - 98 spesifite gösterdiği bilinmekte.
- ELISA ile epidermal transglutaminaz antikorlar (anti-eTG) ise benzer oranlar görülmekte.
DIF ekonomik ve kolay ve hızlı olması nedeni ile altın standart. Titresel değerleri bağırsak tutulumunu değerlendirmekte kullanılabilmekte. Ancak glutensiz diyet sonuçları fazla etkilediği için test öncesi gluten verilerek diyet kaldırılmkata.
Lichen Planus (LP) ve Likenoid reaksiyonlar
LP de son derece kaşıntılı papuler, plaklar deri ve mukozada yer almakta. Lezyonlarda Wickham’s striae belirtisi son derece anlamlı.
DIF de basal tabaka boyunca fibrinojenin tüyümsü paternde depolandığı(dermis-epidermis bileşkesinde inflamasyonu tanımlamakta) görülmekte. Bu alanda "cytoid body" olarak tanımlanan büyük , gruplar oluşturan floresan ile boyanmış yapılar görülmekte. Bu yapılar ölü keratinositler ve hasarlanmış BMZ yapılarını tanımlar. Bu iki yapı DIF te LP için tanısal kriterler. Buna benzer reaksiyonlar likenod reaksiyonlar olarak tanımlanır ve LP dışında epidermal premalign ve malig lezyonlarda, ilaç reaksiyonlarında, eritema multiforme, Steven’s Johnson/toksik epidermal nekroliz, LE, dermatomyositis ve diğer destek doku hastalıklarında görülmekte.
Cutaneous Lupus Erythematosus (LE)
Bullous LE de otoantikorlar tip VII kolajene karşı gelişmekte.
DIF de kaba, granuler antiıkor + kompleman birikimi BMZ boyunca görülmekte.
Deri lupusunun subakut klinik formunda-SCLE DIF de IgG otoantikorların epidermal birikimi görülmekte. SCLE ve DIF de likenoid floresans boyanmada görülmekte.
Lupusta DIF için tam deri lezyonun kenarından sağlam deriyide içine alacak şekilde örnek alınmalıdır(BMZ boyunda bant floresan boyana lupus bant olarak tanımlanır ve bunun nromal deride devamının olup olmasına bakılmalı). Sistemik lupusta deri lezyonunun çevresinde normal deridede lupus bantının devam edebilşeceği unutulmamalıdır.
Vaskülitik otoimmun deri hastalıkları
DIF testleri tanısal amaçlı kullanılmakla birlikte tüm vaskülitlerde DIF pozitif olmayabilir. Bu durumlarda sonraki bölümlerde anlatılacak ANCA testleri yapılmakta.
Küçük damarların tutulduğu vaskülitlerde deri tutulumu ve klinik tuutlum olmakta; palpable purprura, eroziv hemoraji, ürtikeryal plaklar gibi. Orta ve büyük çaplı vaskülitlerde deri belirtileri daha az.
DIF de dermiste damarlar çevresinde IG görülmesi vaskülit tanısı için anlamlı. Buna ek olarak damar çevresinde C3 birikim ve fibrinojen birikimide görülebilmekte.
Dermisin daha yüzeysel damarsal yapılarında vaskülitik IgA boyanması IgA vaskülitleri destekler yada Henoch–Scho¨nlein purpura sendromları ile ilişkili olabilir. Diğer paternler vaskülitiler içim spesifik değildir.
Vakülitiste DIF çalışamları mutlaka taze dopku örneklerinde yapılmalıdır.
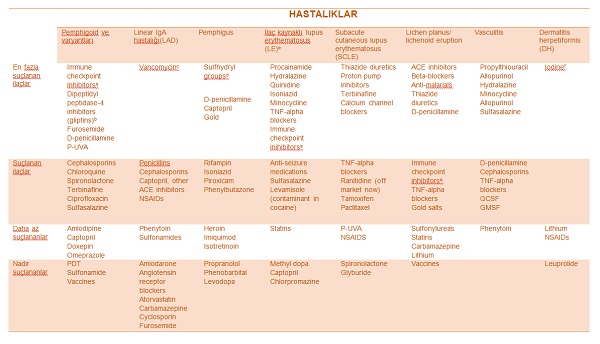
Otoimmun hastalıkların kliniklerinde suçlanan ilaçlar
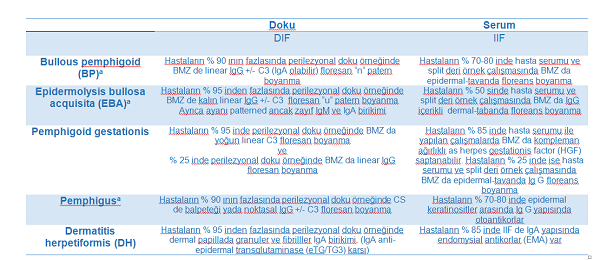
Otoimmun deri hastalıkları tanısında DIF, IFF ve ELİSA özetleri;
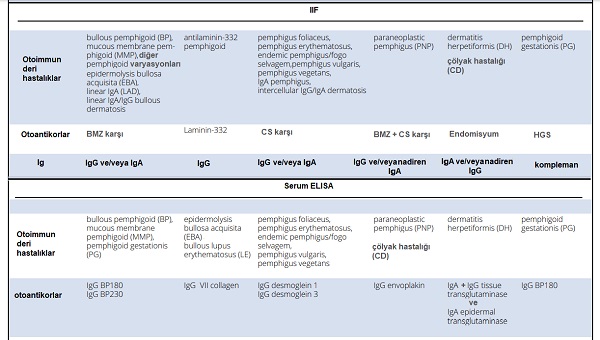
DIF, IIF ve ELISA testlerinde bazı özel durumlar
- DIF in spesifik olamayan bazı bulguları dermatolojik durumlarda görülebilir.
- Biyotin kullanımı ELISA test sonuçlarını etklilemekte.
- İlaçlar örneğin kortkosteroidler Ig seviyelerini düşürmekte, rituximab gibi ilaçlar direct B hücre seviyesini azaltmakta. Bunlar bu test sopnuçlarını etkileyebilir.
- Sınırda yada düşük immünoglobulin seviyeleri,IgA eksikliğinde olduğu gibi, spesifik otoantikorların saptanmasını güçleştirmekte. Dermatittis herpetiformiste IG A seviyelerinde düşüklük olabileceği unutulmamalıdır.
- Ayrıca, düz kas antikorları gibi spesifik antikorlar içeren serumlar, IgG endomisyal antikorlarının saptanmasını engelleyebilir.
- Sistemik lupus eritematozus, sarkoidoz, miyelom ve diğer paraproteinemilerde hipergamaglobulinemi/ immünoglobulin düzeylerinde artış gelişebilmekte buda tanısal testlerde DIF ve IIF'de floresans boyamalarda artışa neden olmakta. Bu görülmesi gereken zayıf florans boyanmasını ve spesifik floresan patern boyanmasını maskeleyebilir.
-
- Ürtiker ve ürtiker reaksiyonları doku örneklerinde bağ dokusu lifleri ve kan damarları çevresinde immünoglobulin veya kompleman birikimi çevresinde eozinofil infiltrasyonu ile fibrinojen birikimi görülmekte. (eozinofiller floresanlı konjugatlarla spesifik olmayan floresan gösterdiği için belirgindir).
- Kronik aktinik değişiklikleri veya diğer fiziksel hasarları olan deri, kutanöz LE'yi taklit eden bazal membran bölgesi boyunca tanecikler, porfiri ve psödoporfirideki bulguları taklit eden kalınlaşmış bazal membran ve perivasküler alanların homojen boyanması ve / veya BMZ antikoru ile ilişkili hastalık veya vaskülitte spesifik bulguların gizlenmesi, elastozun spesifik olmayan floresan vurgulanması ve yüksek arka plan dokusu gibi çeşitli bulgular gösterebilir.
- Kalın lineer BMZ ve kalın perivasküler boyanma, porfiri, psödoporfiri, diğer metabolik durumlar ve güneşe maruz kalma ve diğer fiziksel faktörlerden etkilenen deride gözlenen spesifik olmayan bulgulardır. Porfirin testi ve/veya psödoporfiri ile ilişkili maruziyetler için değerlendirme endike olabilir. Psödoporfiri, ilaç kullanımına, bronzlaşma yataklarından ultraviyole (UV) radyasyona maruz kalmaya, P-UVA tedavisine, kronik böbrek yetmezliğine, hemodiyaliz ve aşırı kola tüketimine atfedilen fotodağılımlı büllöz bir erüpsiyondur.
- DIF yada IIF de yoğun doku boyanması hipergamaglobulinemiyi yansıtabilir. Düşük doku boyaması, düşük IgA veya IgA eksikliği olan hastalarda görülebilir.
- Dokuda pozitif vasküler boyanmanın etyolojisini yorumlamak zor olabilir. DIF ile vasküler boyanma hastalık aktşivasyonu ile ilişkili anatomik lokalizasyonlarda ve belirgin inflamasyon alanlarında spesifik olmayan bir şekilde gözlenebilir. Vaskülitte vasküler boyanma, lezyonun yaşına ve biyopsi yapılan lezyonun içindeki lokalizasyonuna bağlı olarak değişken olabilir.
- Formalin de dahil olmak üzere dokularda proteinleri denatüre edici fiksatörler ile iflerle kısa temas bile DIF bulgularını yanlışlayabilir
- Günümüzde doku biyopsi ve serum örnekleri otoimmun hastalıkların tanısal testler için kaynak material olarak kullanılmakta. İmmünolojik gelişmeler ve testlerin duyarlılığı arttıkça, tükürük, bül sıvısı, idrar ve saç gibi doku örnekleri(doku bütünlüğünü bozmadan) tanısal amaçlı ve tedavi takiplerinde kullanımı umut vaat etmekte. Örneğin son yıllarda MMp hastalığında tüktükte ELISA BP180 NC16A IgA ve IgG antikor seviyelerine bakılabilmekte. ları, MMP için yararlı bir tanısal biyobelirteçtir. Topikal antikor reaktanları veya diğer hastalık belirteçleri ile cildin konfokal mikroskopisine benzer şekilde yerinde analizler ve "bakım noktası" testi de dahil olmak üzere bant sıyırma analizleri geliştirilebilir.
Otoimmun deri hastalıklarında testler
ANA
Otoimmun deri hastalıklarında en yaygın kullanılan test ANA testidir. Otoiimun hastalık düşünülen hastanın serumu HEp-2 hücre ve dokusu içeren slaytlar üzerine konulmakta. cells or tissue. Hasta serumunda otoantikorlar var ise slayt üzerindeki antijenlere bağlanmakta. Sonra antikor spesifik ve floresans ile işaretlenmiş antikorlar - Ig G eklenmekte. Bunlarda slayt üzerindeki antijen-antikor kompleksine bağlanmakta. Bu slaytlar floresan mikrokop ile incelenerek floresanın boyanma paterni ve titresi değerlendirilmekte. ANA fluoresan boyanma paterni nüklear, sitoplazmik ve mitotik olarak 3 gruba ayrılmakta. Bu boyanma ve paternler hastalıkların için spesifiktir. Mitotik boyanma henüz hastalılar için ilişklilendilememiştir. Aşağıdaki ilk grafikte https://anapatterns.org alınmış paternler, ikinci grafikte paternler ile klinik arasındaki korelasyon için örnekler görülmekte.
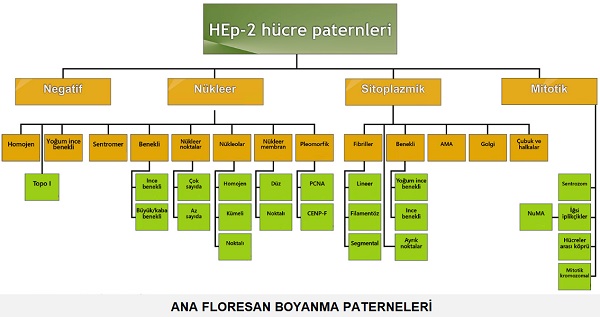
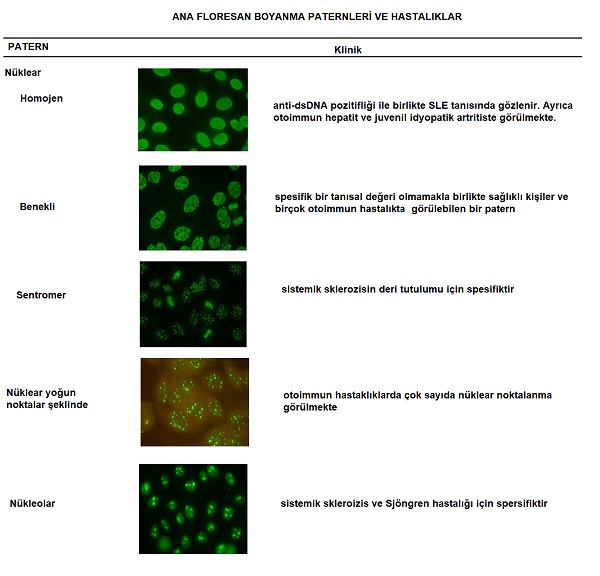
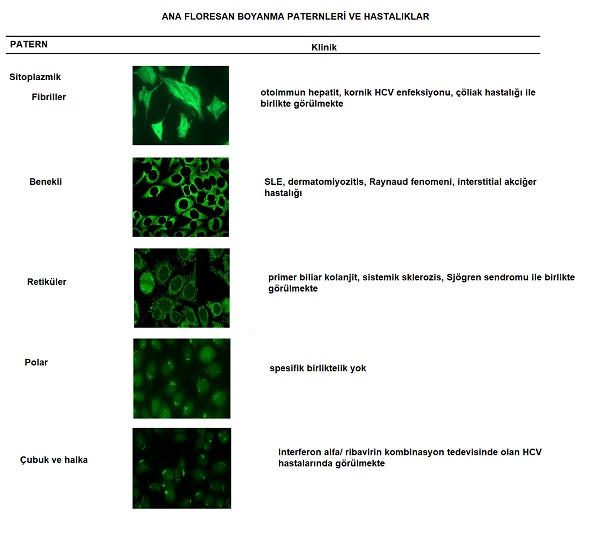
ANA ile seri titrasyon oran testleri ile farklı dilüsyonlarda sonuçlar elde edilebilmekte. Dilüsyonal test sonuçları otoimmün deri hastaıklarının takibinde ve tedavilerin kontrolünde kullanılmakta. Ayrıca ANA floresan testlerinin otoimmun bir hastalık olmaksınzın sağlıklı kişilerde % 20-30 oranında pozitif olabileceği unutulmamalıdır. Titrasyon değerleri 1:160 üzerrinde olduğunda daha anlamlı pozitif osnuç olarak tanımlanmakta
Multiplex immunoassay testleri
Otoimmun deri hastalıklarında kullanılan diğer bir test hasta serumunda aynı anda çok sayıda otoantikorların saptanmasını sağlayan "Multiplex immunoassay" testleridir. Bu test ile otoimmun hastalıklarda en sık gözlenen otoantikorlar saptanabilir. Bu testlerin hastalıklarar göre duyarlılıkları % 58-79 arasında değişmekte. laboratuvar maliyetleri ve ücretlendirmeleri daha pahallıdır.

Hasta şikayetleri ve muayene klinik bulgularından yol çıkılarak otoimmun bir deri hastalığından şüphe duyuluyor ise;
- ilk olarak ANA testi yapılmalı. İmmunofloresan ANA için altın satandart. Ancak immunofloresan ANA testleri(laboratuvarlar arasında standartları değiştiği için) sadece SLE yüksek klinik şüphesi olan bir hastada multiplex immunoassay testler negatif ise yapılmalıdır. Ancak immunofloresan ANA testinin multiplex immunoassay test sonuçlarından daha değerli oldukları unutulmamalıdır. Örneğin anti-ds DNA testi pozitif iken immun floresan ANA negetif daha anlamlı bir sonuçtur.
- ANA pozitif ise alt gurubunda yer alan bu antikor testleri istenmelidir.
- ANA test tekrarları sadece titrasonu ile hastalığın aktivitesinin takibinde yaptırılabilir. SLE klinik aktivitesinin takibinde kompleman çalışmaları yapılabilir ancak enfeksiyon ve otoimmun durumlarda düşük C3 ve C4 seviyeleri olabileceği untulmamalıdır.
Antinötrofil Sitoplazmik Antikor - ANCA Testleri
Otoimmun deri hastalıkları klinik ve deride patolojik etkileri ile küçük -orta çaplı damarların inflamasyonundan-vaskulit kaynaklanabilir. Vaskülitk deri hastalıkları deriden kabarık yada deri seviyesinde purpura, papulonekroitk lezyonlar, atipik ülserasyon gösteren purpuralar ile seyretmekte. Vaskülitik hastalıkların tanısı, klinik ve tedavi takiplerinde ANCA testleri kullanılmakta.
ANCA indrekt immunofloresan testleri için hasta serumu ethanol ile fikse edilmiş nötrofiller ile enkübe edilmekte.Floresan ile işaretlenmiş IgG eklenerek floresan mikroskop altında nötrofillerde boyanmaya, bu boyanmanın paternine ve titresine bakılmakta.
ANCA floresan paternler;
- sitoplazmik (c-ANCA); pozitif c-ANCA sitoplazmada diffüz floresan boyanma olmakta ve sıklıkla PR3 antikorları ile birlikte. c-ANCA testleri granulomatosis ve polianjitis için % 77-65 oranında duyarlı ve % 97-98 oranında spesifiktir.
- perinüklear (p-ANCA); pozitif p-ANCA nükleus çevresinde ve nükleusa doğru boyanma olmakta ve MPO antikorları ile birlikte. p-ANCA testleri polianjitis için %85-89 oranında daha yüksek bir duyarlılık göstermekte.
- atipik perinüklear (atipik p-ANCA); atipik p-ANCA da nükleus çevresinde ancak nüklleusa uzanmayan boyanma olmakta ve nöytroifil antijenkleri olan katalaz, elastaz, ve lizozimlere karşı antikorlar ile bilrikte.
İmmunfloresan ANA boyanmaları özellikle p-ANCA paternini maskeleyebilir.
ANCA testleri öncesi proteinaz 3 PR3-ANCA ve myeloperoksidaz MPO ANCA test taraması yapılmalıdır.
Vaskülit ile seyretmeyen bazı otoimmun hastalıklarda; SLE, otoimmun artritis ve inflamatuar bağırsak hastalıkları-IBD, ANCA lar pozitif olmakta.
Atipik p-ANCA sistemik vaskülitik hastalıklarda p-ANCA ya göre daha az birliktelik göstermekte. Buna karşın atipik p-ANCA ülseratif kolit gibi imflamatuar hastalıklarda daha sık görülmekte.
ANCA titreleri hastalığın aktivitesi ile korelasyon gösterdiği için klinik ve ve tedavi takiplerinde seri titre takipleri yapılabilir.
Myositis İle Birlikte Olan Derinin Otoimmun Hastalıklarında Testler
Otoimmun bir hastalık olan dermatomyositis ve polimyositis gibi hastalıkların tanısı ve klinik alt grupların saptanmasında kas dokusunun tutulumu ile birlikte myositis spesifik antikorlar-MSA testleri yapılabilir. MSA antikor profili bunun dışında hastalığın klinik sürecinde maligniteler ve organ-sistem tutulum risklerinide göstermekte. Örneğin anti-MDA-5 pattern dermatomyositiste klinik olarak papüller ve hızla ilerleyen ülserasyonları tanımlarken akciğer intertisyel tutulum riskinin yüksekliğini ifade etmekte.
MSA antikrolar;
- Anti-Jo1; antisentetaz sendromları(artritis, myositis ve intertisyel akciğer tutulumunun olduğu 3 kliniğin standart olarak olduğu tablo) antikorları ile birlikte görülmekte. Bunun pozitif olduğu hastalarda klinik olarak deri lezyonları Gottron papulleri ve heliotrope döküntülerdir.
- Anti-Mi2; bunun pozitif olduğu hastalarda klinik olarak deri lezyonları Gottron papulleri, heliotrope, shawl sign ce fotosensitivitedir. Kas tutulumu simetrik, proksimal kas grubunu etkileyen ve kortikosteroidklere cevap veren özelliklerde. Prognoz genellikle iyi; malignite ve intertisyel akciğer tuutlumu düşük.
- Anti-TIF1 (eski adı anti-P155/140); MSA antikorları içerisinde beyaz ve batı ırklarında en sık görülen, Asya ırklarında nadır. Bu antikor pozitifliği klinik olara deri bulgularının şidretli olacağını göstermekte(fotoeritem, psoriasis benzeri lezyonlar, palmar hiperkeratozis, verru benzeri papüller...). Ayrıca antikorun varlığı %78 oranında malignite gelişebilme riskini tanımlamakta.
- Anti-MDA5 (Anti-melanoma differentiation-associated gene 5, eski adı CADM-140); pozitifliği genellikle amyopatiyi yani kas tutulumu olmadan deri tutulumlarının olacağını desteklemekte(mukokutanöz ülserasyobnlar, palmar papüller, pannikulitis, diffüz alopesi...). Antikorun pozitifliği deri lezyonlarında ülserasyonların kolay gelişebileceğini ve intertisyel akciğer tututlum riskinin yüksek olduğunu göstermekte.
- Anti-NXP2 ; sıklıkla juvenile dermatomyositis ile birlikte. Pozitifliği with calcinosis cutis, şiddetli miyopati ve kötü prognozu göstermekte. Erişkinlerde pozitif olması malignite riskini desteklemekte.
- Anti-SAE; pozitifliği ileri yaşlarda geçe ve şiddetli başlayan dermatomyositis desteklemekte ve deri bulguları nerede ise hiç yok.
Bunlar içerisinde sadece anti-Jo1 test sonucu hastalık tanı kriteri olarak kullanılmakta.
İnflamatuar Bağırsak Hastalıkları-IBD
IBD hastalılarında deri mukozal belirtiler sık görülmekte. Pyoderma gangrenosum, eritema nodosum, Sweet sendromu, aftöz stomatitis, pyostomatitis vejetans gibi. Bunların varlığı ile IBD düşünüldüğünde tanısal olarak endoskopi altın standart.
Anti-saccharomyces cerevisiae antikorları(ASCAs) Kron hastalığında serolojik bir marker olarak saptanmıştır. Bu antikor genç kron hastalarında, kronun ileum tutulumunda görülmekte ve sıklıkla darlık risklerini tanımlamakta.
IgG ASCA ELISA testleri %84-41 duyarlılık ve % 96-86 spesifiklik göstermekte.
IgA ASCA ELISA testleri ise %84-34 duyarlılık ve % 95-84 spesifiklik göstermekte. Birlikte yapıldığında duyarlılık % 51-92 çıkmakta.
ASCA pozitif ve p-ANCA negatif ise duyarlılık % 55 ce spesifiiklik % 93 olmakta.
Kron ve ülseratif kolit gibi IBD larında fekal, moleküler ve serolojik testler kullanılmakta. Bunlar içerisinde fekal "calprotectin" düşük ekonomik maliyet, yüksek duyarlılık ve spesifiklği ile en fazla kullanılan test. İnflamatuar bağırsak hastalıklarında nötrofiller tarafından bağırsak içerisine "calprotectin" salınmakta(kolitlerdede görülmekte). Calprotectin IBD aktivasyonun değerlendirilmesinde kullanılmakta. hastalığın aktvitesinde feçeste 7 gün saptanabilmekte. % 76% duyarlılık ve % 92 spesifite ile değerli bir test. Endoskopi yapılmadan önce taram testi olarak kullanılmakta.

