- Gösterim: 146096
Cilt, yaklaşık 2 m²'lik yüzey alanı ile vücudumuzun en büyük organıdır. Mikroorganizmalar, kimyasallar, toksinler, UV ve radyasyon gibi çevresel etkilere karşı en dış bariyeri oluştururken, çevre ile vücut arasındaki hemostazı sağlamaktadır. Cildin bütünlüğünün bozulup hasarlanması, mikroorganizmalar, sıcak-soğuk, güneş, kesici-batıcı bir cisim veya kimyasal bir madde gibi herhangi bir dış etkenle olabileceği gibi, vücut-deri hastalıklarına bağlı olarak içsel nedenlerle de gelişebilmektedir. Cildin hasarlanması ile kusursuz çalışan bir mekanizma devreye girmekte; bu mekanizma fizyolojik yara iyileşmesidir. Fizyolojik yara iyileşmesi, doku bütünlüğü ve fonksiyonunu tekrar sağlayan hücresel ve biyokimyasal mekanizmalardan oluşmaktadır. Yara iyileşme bozuklukları, patolojik yara iyileşmesi olarak tanımlanır. Patolojik yara iyileşmesi, sıklıkla farklı klinik özelliklere sahip olan skar ve nedbe izi gelişimi ile sonlanmaktadır. Tanım olarak, yara izleri (Latince: cicatrix) ciltte dermisin derin katmanlarını içeren patolojik yara iyileşmeleridir. Cilt seviyesinin altına çökmüş lezyonlar atrofik yara izleri olarak görülebildiği gibi, deriden kabarık hipertrofik yara izleri ve keloidler gibi aşırı doku büyümesi ile karakterize olabilmektedir. Kozmetik sorunlara ek olarak, genellikle fonksiyonel bozukluklara da neden olabilmektedir. Patolojik yara iyileşmesi, ekzojen ve endojen faktörlerden etkilenebilir; lokal nedenlere (enfeksiyon ve kan dolaşımı) ek olarak, sistemik faktörler de önemli bir rol oynamaktadır (sistemik inflamasyon, metabolik, endokrin ve onkolojik hastalıklar). Patolojik yara iyileşmesinde sigara kullanımı ve beslenme gibi bireysel yaşam tarzı alışkanlıkları da önemlidir. Patolojik yara iyileşmesi ve skarlar, dünya çapında sağlık sistemleri üzerinde önemli bir etkiye sahiptir.
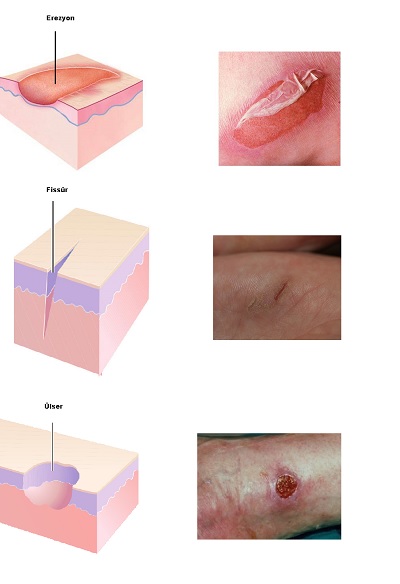
Ciltte yaralanma, doku hasar derinliğine göre erozyon, ülser ve fissür olarak tanımlanır. Erozyon, deride yüzeysel doku kayıplarını tanımlarken, fissür ya da çatlak, deride dikey yaralanma ile doku kayıplarını tanımlamaktadır. Ülserler ise cilt yüzeyinden dermise kadar olan derin doku kayıplarını tanımlamaktadır.
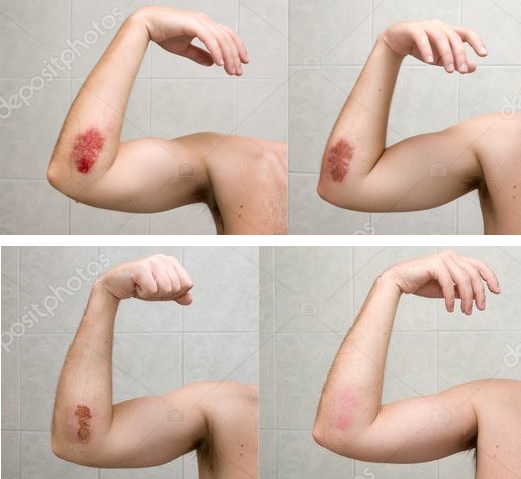
Cilt dokusunun bütünlüğünün kaybı ve yara dokusunun oluşumu fizyolojik yara iyileşme süreçlerinin başlamasına yol açar. Cilt yaralarının iyileşmesi için kesin bir süre verilemez. Bu süre kişinin genel sağlık durumuna, kan dolaşımına, yaranın oluşma nedenine, vücutta yerleşim yerine, yaranın türüne, yarada enfeksiyon olup olmamasına... gibi değişken birçok değişkene bağlıdır. Yani, her yara kendi özelliklerine göre iyileşir. Ancak 3 aydan daha uzun süren yaralar kronik yara olarak tanımlanmaktadır. Yara iyileşmesi doku bütünlüğünü yeniden sağlamayı amaçlar. Ancak bazı durumlarda, patolojik yara iyileşmesinde doku bütünlüğü tam olarak sağlanamaz. Doku iyileşmesi uzayabileceği gibi sonrasında skar-nedbe-iz gelişebilir ve fibrozis (normal dokunun yerini destek dokusunun alması) oluşumuyla sonlanır.
Fizyolojik Yara İyileşmesi
Yara iyileşmesi, dokuda hücreler ve aracıların karmaşık bir etkileşimi ile ardışık ve örtüşen bölümlerden oluşmaktadır. Yara iyileşmesi sadece yara bölgesiyle sınırlı değildir; tüm vücudu kapsayan hücresel, fizyolojik ve biyokimyasal olaylar bütünüdür. Başarılı bir fizyolojik yara iyileşmesi, yara bölgesinde inflamasyon yapıcılar ile inflamasyon önleyiciler ve doku yıkıcılar ile doku onarıcılar arasındaki dengedir.
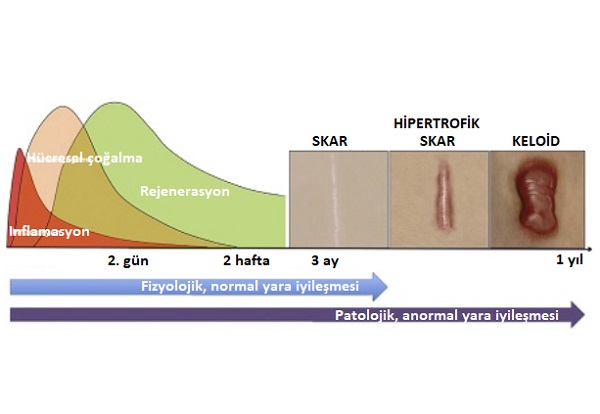
Yara iyileşmesi temel olarak ardışık ve örtüşen üç aşamada gerçekleşir.
1. Hemostaz ve inflamasyon safhası(1-5 gün sürmekte)
2. Proliferasyon-Hücresel Çoğalma Safhası (5-14. günler)
3. Maturasyon-Doku Olgunlaşması Safhası (14. günden sonrası)
İnflamasyon, hemostaz safhası
İnflamasyon fazı, yara iyileşmesinin başlangıcını işaret eder. Cilt hasarının olduğu alandaki yerleşik hücrelerin aktivasyonu ve kan dolaşımındaki hücrelerin yaraya alınması ile karakterize edilir. Yara dokusunda inflamatuvar reaksiyon hemostazdan önce gerçekleşir. Dokuda kanama ve damarsal bütünlüğün korunması hemostaz ile sağlanır. Hasarlı doku damarlarında salınan subendotelyal kollajen, pıhtılaşma sürecinin içsel ve dışsal yollarını aktive eder. Yaralanmayı takiben yara bölgesindeki yıkıma uğramış damarlar hemen daralır.Damar duvarı zedelendiğinde trombositler (kan hücrelerinden kanama ve doku onarımında görevli) açılan damar duvarındaki kollajenle temas ederek aktive olurlar. Böylece hem damar duvarına hem de birbirlerine yapışırlar. Trombositlerden hasarlı dokuya doku ürünleri salınır. Bunlardan Tromboksan A2’nin aktivasyonu ile trombositler geçici ilk pıhtı tıkacını oluşturarak başlangıçta kanamayı azaltırlar. Daha sonra bu tıkaç içerisinde fibrin oluşumu ile kalıcı pıhtı oluşmaktadır. Hemostasis düzenlemek için fibrin pıhtısı nötrofiller ve monositler için iskelet görevi yapar. Daha sonraki aşamada trombositlerden salınan serotonin ve diğer damar daralma-vazokonstriktör ajanlarla vazokonstriksiyon gelişerek kanama azalır. Başlangıçta gelişen damarlarda daralma prostaglandin ve kompleman sisteminin aktivasyonu ile yerini yaygın damarlarda genişleme-vazodilatasyona bırakır. Genişlemiş damarlar doku hasarlı alana kan hücrelerinin geçişini arttırmakta ve hücreler arasında inflamatuar eksuda toplamakta. Kollajen, trombosit, trombin ve fibronektin ile birlikte diğer hücresel bileşenlerden oluşan bir pıhtı, sitokinler ve büyüme faktörleri tarafından çeşitli hücrelerin (nötrofiller, monositler, fibroblastlar ve endotel hücreleri) alana gelerek yerleştiği geçici bir matris oluşturur. Aynı zamanda, kompleman sistemi ve bağışıklık sistemi aktive edilir. Doku zedelenmesi dokuda birçok kimyasal mediatör ve hücreler arası bilgi aktarımını sağlayan sitokinlerin salınımına neden olur. Bu maddeler yara dokusu ve çevresinde aktivasyon ve inhibisyon yaparak birçok kompleks olayı başlatır.
İnflamatuar faz, yara iyileşmesinin başlangıcını işaret eder ve birincil hemostaz, yerleşik hücrelerin aktivasyonu ile dolaşan hücrelerin yara alanına alınmasıyla karakterizedir.
Bağışıklık sisteminin bir parçası olan nötrofiller, erken inflamatuar fazın başlıca aktörleridir. Hasarlı dokuda ortaya çıkan interlökin (IL)-1, tümör nekroz faktörü (TNF)-α, dönüştürücü büyüme faktörü (TGF)-β, trombosit faktörü 4 ve var ise bakteriyel bileşenler, nötrofilleri dolaşım sisteminden hasarlı dokuya çekmektedir. Eş zamanlı olarak, hücre yüzey deseni tanıma reseptörleri (PRR'ler), istilacı mikroorganizmalar (patojenle ilişkili moleküler desenler, PAMP'ler) ve hasarlı dokudan (hasarla ilişkili moleküler desenler, DAMP'ler) gelen ekdış tehlike sinyallerini tanır. Bunu inflammasom ve kaspaz aktivasyonu ile inflamatuar sitokinlerin (IL-1 dahil) salınmasıyla bir sinyal yolunun tetiklenmesi izler. Salınan mediatörler vazodilatasyona yol açar ve nötrofiller başta olmak üzere kan hücrelerinin yara bölgesine göçünü artırır.
Daha sonra yara alanına monosit isimli kan hücreleri hakim olmaya başlar. Yaralanmadan 72 saat sonra hakim olan hücreler makrofajlardır. Dolaşımdaki monositler dokuya geçtiklerinde makrofajlara farklılaşır, yerleşik hale gelirler ve diğer hücrelerin işlevini düzenlerler (fibroblastların uyarılması, keratinositlerin aktivasyonu), anjiyogenezi desteklerler ve yara debridmanına katkıda bulunurlar. Makrofajlar, diğer faktörlerin yanı sıra TGF-β tarafından aktive edilir ve yara iyileşmesinin farklı zaman noktalarında farklı sitokin salınımları ile farklı işlevsel programlar üstlenirler. Erken makrofaj popülasyonları (M1 alt kümesi) inflamatuar özelliklere sahipken, yara iyileşmesinin sonraki aşamalarındaki makrofajlar fibroblast farklılaşmasını destekler (M2 alt kümesi). Bu denge, başarılı ve fizyolojik yara iyileşmesi için çok önemlidir ve patolojik yara iyileşmesinde başlangıç noktası olabilir.
İnflamasyonun yara iyileşmesinde bazı tartışmalar var. Anne rahmindeki bebekte-fetüste yaralanmalar sonrası inflamasyon fazı erişkine göre daha kısadır ve yara iyileşirken skatris gelişmemektedir. İnflamasyon yara iyileşmesinde ik aşama ancak kısa süreliolması skatris gelişimini önleyebilir. Son zamanlardaki dokuda bir sitokin olan aktive protein C (APC)'nin yarada inflamasyon sürecini baskıladığı, anjiogenezi stimüle ettiği ve dermisin yeniden büyümesi ve epidermal rejenerasyonu sağlayarak yara iyileşmesini hızlandırdığı gösterilmiştir.
Proliferasyon-Hücresel Çoğalma Fazı
İnflamasyon ve proliferasyon evresinden sonra yarada yavaş yavaş bu faz başlar ve yara iyileşmesi ile stabilitesi için kritik öneme sahiptir. Yara iyileşmesinin en uzun süren aşamasıdır. Yara iyileşmesinin her aşamasında olduğu gibi, bu aşama da diğerleriyle üst üste binmiştir. İnsanlarda yara matürasyonu, klinik olarak, yara kontraksiyonu—alanın büzülerek daralması, kızarıklık ve yara kalınlığında azalma, ve yara kuvvetinde artma ile karakterizedir. Matürasyon fazında yara kalınlığı azalırken, yaranın gerilmeye dayanım kuvveti ters orantılı olarak artar.
Kollajen üretimi yaralanmadan sonra ortalama 21. güne kadar sürekli bir artış gösterir. Bu aşamadan sonra kollajen sentezinde bir azalma gözlenir. Yara iyileşmesinin 21. gününde maksimum kollajen miktarına ulaşılsa da, yaranın tensil kuvveti normalin ancak % 20’si kadardır. 6. Haftada yaranın tensil kuvveti, olması gerekenin % 80’ine ulaşır. 21. günle 6. hafta arasında geçen ve yara kuvvetinin arttığı bu dönemde gerçekleşen asıl olay, kollajen yıkımı ve yeniden düzenlenmesidir.Yara iyileşmesinin erken dönemlerinde kollajen fibrilleri düzensiz şekilde dizilmişlerdir. Bu, iyileşmenin erken döneminde, yüksek kollajen miktarına rağmen, yara kuvvetindeki zayıflığı açıklar. Birkaç aydan birkaç yıla kadar süren bir süre boyunca tip III kolajen, tip I kolajen liflerinin kalın demetleriyle değiştirilir.
Bu dönemde kolejen dışında glikozaminoglikanlar da yapılmaktadır. Yarada bulunan ana glikozaminoglikanlar dermatan ve kondroitin sülfattır.Fibroblastlar yara iyileşmesinin ilk 3 haftasında konsantrasyonları arttırarak bu bileşenleri sentez ederler. Fibrillere ve fiberlere kollajen subünitlerinin bağlanmasının sülfatlanmış proteoglikanlarca üretilen kafeslere bağımlı olduğu öne sürülmektedir. Sülfalanma derecesinin kollajen fibrillerinin konfigürasyonunun belirlenmesinde kritik öneme sahip olduğu izlenmektedir. Yara iyileşmesinin ileri zamanlarında proteoglikan içeriği kademeli olarak azalır.
Bu evrede remodelling başlar, bu da kollajenin ve glikozaminoglikanların reorganizasyonu ile ilişkilidir. Kollajen matriks MMP'lertarafından yıkılır, son yara yeri kollajeni kollajenolizis ve kollajen yapımı arasındaki denge sonucu şekillenir. MMP ler kollajen yanısıra elastin, laminin, fibronektinin hidrolizini katalize eder ve sitokin ve büyüme faktörlerini de işler. Normal ve bütünlüğü korunmuş deride MMP'lerçok düşük miktarlardadır. MMP-7 ve MMP-19 sadece ter ve yağ bezlerinde sürekli olarak üretilir.Kollajen sentezi ve yıkımı sitokinler ve büyüme faktörleri tarafından denge halinde tutulur. TGF beta gibi bazı sitokinler hem yapım hem de yıkımda görev alabilirler. Gap junction protein connexin 43 (Cx43) yara iyileşmesi, re-epitelizasyon, ekstraselüler matriks oluşumuna rolü vardır. Cx43’ün mekanizması tam olarak bilinmese de özellikle TGF-beta sinyalizasyonunu ve fibrozisi düzenlediği, hafif dereceli sikatris formasyonuna yol açtığı bilinmektedir.
Granülasyon dokusu stabil skar dokusuna dönüşür. Bu süreçte yerleşik hücreler programlanmış hücre ölümüne (apoptozis) uğrar. Hücre rejenerasyonu ve yıkımı(degradasyonu) arasındaki denge bozulduğunda aşırı doku üretimi meydana gelir(fazla gelişen skar dokusu, hipertroifk skar gibi).
Skar matürasyonuyla beraber, klinik olarak gözlemlenen kızarıklık azalışı yara içindeki yeni damarlanma yoğunluğunun değiştiğini gösterir. Matür skar, granülasyon dokusuna oranla daha az damarlanma içermektedir.
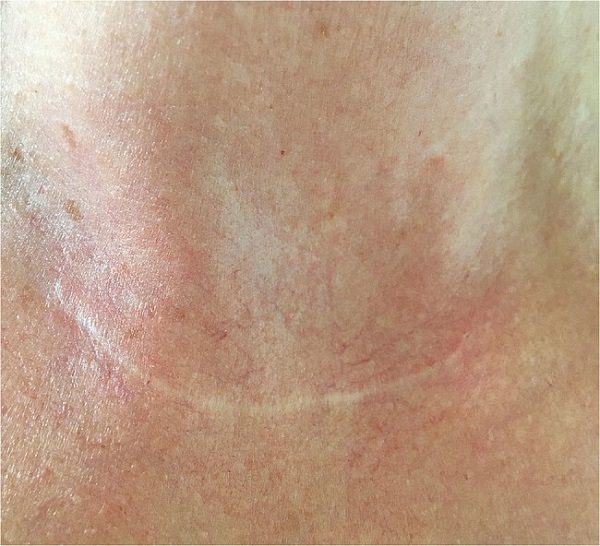
Yara iyileşmesi, dokunun yeniden yapılandırılması, ve dermoepidermal yapısal birimin orijinal şekline ve stabilitesine sahip olmadığı karakteristik bir kolajenöz bağ dokusu bileşimine sahip bir normal skar oluşumuyla sonuçlanır.
Deri iyileşmesinde en önemli süreç aslında deri epitel hücrelerinin epiteliyal mezenkimal dokuya geçişidir. Deride epitel ve mezenkimal hücrelerden ibarettir. Deri eitel hücreleri meznkimal dokuya geçerek fibroblast, kan damarlarının düz kas hücreleri, perisitler gibi mezenkimal hücrelere farklılaşırlar. Bu farklılaşmada deri epitel hücrelerinde moleküler değişiklikler ile mezenkimal fenotip gelişir. Bu değişim bu hücrelere mezenkimal dokuya göç etme kapasitesi, apopitoza direnç ve mezenkimal hücreler arası matriksin üretim özelliği sağlar. Dokularda üç tip epitel-mezenkimal geçiş bilinmektedir. Tip 1 embriyogenezis sırasında dokular oluşurken dermal fibroblastlarda, Tip 2 erişkinlerde remodelling ve fibrozis sırasında ve Tip 3 kanser hücreleri fenotipik dönüşümle hareketlilik kazanıp metastaz yaparken gözlenir. Yara iyileşmesinde önemli olan Tip 2 epitel-mezenkimal geçiştir. Bu geçişte yapılan moleküler incelemelerde bu geçişi sağlayan bazı mekanizmalar (BMP, Wnt, Notch/Delta, ve Hedgehog gibi) belirlenmiştir.
Yara iyileşmesinde derinin üzerinin kapanması, yani epitelizasyon, önemlidir. Bu, yaraya bitişik epitel hücrelerinin yara merkezine doğru proliferasyonu ve migrasyonu ile ilişkilidir. Yaralanmanın 1. günü yara kenarındaki epidermis kalınlaşır. Yara kenarındaki marjinal bazal hücreler alttaki dermise olan bağlantılarını kaybeder, genişler, ve geçici matriksin yüzeyine doğru hareketlenir. Yara kenarındaki hücreler hızla prolifere olup birbirleri üzerinden hareket ederek (yara alanına doğru) yara defektini kapatırlar. Bu süre hafif yaralarda 48 saatte tamamlanır ancak daha büyük defektli yaralarda bu süre uzar. Bu sürecin kontakt inhibisyon kaybı ile fibronektin ve immün monomoleküler hücrelerden salınan sitokinlerce kontrol edildiği bilinmektedir. Özellikle EGF, TGF-Beta, PDGF, ve IGF-1 bu sitokinlerin başlıcalarıdır.
.

