- Gösterim: 16232
Ülkemizde estetik uygulamaların yıllık istatistik verileri maalesef sağlıklı değil (her konuda olduğu gibi). ABD verilerine bakıldığında; 2020 yılında (COVID-19 pandemisine rağmen) 15.6 milyon kozmetik uygulama yapıldığını görmekteyiz (2.3 milyon cerrahi uygulama, 13.2 milyon cerrahi olmayan uygulama). Cerrahi uygulamalar sırasıyla burun estetik cerrahisi, göz kapaklarının estetik cerrahisi, yüz germe, liposakşın, meme estetik cerrahisi… Cerrahi olmayan uygulamalar sırasıyla botulinum toksin uygulamaları, dolgu uygulamaları, kimyasal peeling, lazer yüz gençleştirme… Tüm uygulamalarda %92 oranı ile kadınlar erkeklere göre açık ara önde. Uygulamaların yapıldığı yaş dağılımı 30-70 yaş dönemi. 2020 yılında 1 hastanın botulinum toksin için ortalama 408 dolar, dolgular için ortalama 4751 dolar ödediğini görmekteyiz. Bu rakamlar hasta sayıları ile çarpıldığında inanılmaz rakamlar çıkmakta. Bunu bir de TL'ye çevirdiğinizde... Estetik-kozmetik uygulamalar ve ürünler hızla büyüyen bir ekonomik sektör. Kullanılan ürünlerin birim fiyatları; kartelleşmiş üretici firmaların ücretlendirme politikaları, distribütör firmaların kar payları, kur farkı ve uygulayan doktor ücreti derken çok artmakta (düşük maliyetler için yasal kullanım onamı olmayan ürünleri hastalarımıza kesinlikle kullanamayız). Bir hasta için kullanılması gereken ürün sayısı arttıkça yükselen maliyetler hastalar ile biz doktorları karşı karşıya getirmekte. Diğer taraftan kullandığımız ürünlerin klinik ve estetik etki sürelerinin kalıcı olmaması, bu süreler sonunda tekrarlanması zorunluluğu, sentetik olmaları, üretimleri aşamasında içeriklerinden ya da hastadan kaynaklanan düşük oranlarda da olsa gözlenen yan etki riskleri ve her geçen gün artan maliyetler gibi büyüyen sorunlar...
Bu olumsuzluklar cerrahi olmayan estetik uygulamalarda yeni çözüm yollarının ve ürünlerin gelişmesini sağladı. Son yıllarda hastanın kendi dokularından elde edilen dokular ve doku ürünleri kullanılmaya başlandı. Deri fibroblast kültürleri, PRP, yağ dokusu transferleri, yağ dokusu kaynaklı SVF enjeksiyonları ilk akla gelenlerdir. Bunlar için "endojen rejeneratif teknolojiler - endogenous regenerative technology - Endoret" tanımlaması kullanılmaktadır. Endoret sadece estetik girişimlerde değil, ağız ve çene cerrahisinde, travmatolojide, ortopedi hatta kalp damar cerrahisinde geniş bir kullanım alanı bulmuştur.
Dermal dolgular yerine kullanılabilecek; mikroyapısı uygun, biyomekanik özellikleri (reolojileri) dolgular ile benzer olan, biyoyaralanma oranı yüksek, biyolojik olarak aktif, düşük maliyetli ve daha az yan etki riski içeren kanımızdan elde edilen doku jellerinden bahsetmeye çalışacağız. Bu kandan elde edilen, lökosit içermeyen, plateletten zengin ve platelet kaynaklı büyüme faktörleri içeren kan plasması fibrini olarak tanımlanmaktadır (leukocyte-free plasma rich in growth factors; PRGF). PRGF jel formu dokuya uygulandığında yüksek bir volüm stabilitesi sağlamakta, mikroyapısının mekanik stabilitesi oldukça yüksek, vizköz yapısı ile doku defektlerinde volüm amaçlı rahat kullanılmaktadır. Bu nedenle sentetik dolgular gibi yüzde kırışıklıklar ve katlantıların görünümlerinin yumuşatılması ve yok edilmesi, yüzde istenilen estetik alanlara volüm verilmesi ve özel uygulama alanları ile yüzde germe-lift etkisi ile kullanılmaktadır. Ayrıca içeriğinde platelet kaynaklı biyolojik aktif maddeler ile doku onarımı ve gençleşmesini gerçek anlamda sağlayan biyoaktif özellikler de bulunmaktadır. PRGF jel kozmetik kullanımı dışında, uygulama alanında 3-6 ay sebum salınımını düzenlemekte, deri gözeneklerinin sayı ve boyutunu azaltmakta (bu etkinlikleri ile akne, seboreik dermatit gibi cilt hastalıklarında da kullanılmakta), deride lekelerin kızarma ataklarını kontrol altına aldığı gösterilmiştir.

PRGF jel hazırlanması için yine birçok firma ve bunların ürettikleri kitleri görmekteyiz. Burada özel bir kit kullanmaksızın PRGF jelin elde edilmesini anlatırken neden-niçin ilişkisini de detaylandırmaya çalışacağız.
Kan alımı ve PRGF jel hazırlanırken vakum tüplerde kullanılabilir. Ancak luer lock enjektörler, kanın alınmasından jelin hazırlanmasına kadar kontrollü kapalı bir sistem oluşturması ve pratik olması nedeniyle tercih edildi. Bir marka önerisi olmadan enjektör seçiminde, pistonu üzerinde kesilmesini-kırılmasını sağlayan çentiği olan steril tek kullanımlık 10 ml'lik luer lock enjektörler kullanıldı. 10 ml enjektörlerin çapları basit ya da kompleks santrifüjler için uygundu.

Enjektöre 1,5 ml sodyum sitrat çekilir. Üzerine venöz kan 9 ml alınarak 10 ml tamamlanır. Venöz kanın alınmasında kelebek seti kullanımı, daha fazla enjektör hazırlanmasını kolaylaştırmaktadır. Enjektör içerisinde sodyum sitrat ve kanın karışımı için enjektör birkaç kez ters düz edilir. Luer lock kapağı takılarak (bunun yerine insülin iğnesi de kullanılabilir) piston çentikten kesilir. 10 ml enjektör, çap ve boyut olarak santrifüj için kullanıma uygun hale gelir. Tek bir enjektör ile PRGF hazırlanacaksa, başka bir 10 ml luer lock enjektöre 10 ml SF çekilerek piston çentikten kesilir ve luer lock kapağı takılır. Bu enjektör, santrifüj sırasında dengenin sağlanması için kullanılır. Enjektörlerin santrifüje bu şekilde yerleştirilmesi, plasmanın alınmasını kolaylaştırmaktadır.

5 dakika 580 g de santrifüj uygulanır. Santrifüj skalasında g yerine rpm kullanılıyorsa http://www.endmemo.com/bio/grpm.php sitesinden santrifüj markanıza göre g'nin rpm karşılığını bulabilirsiniz. Santrifüj sonrası enjektörde; en altta eritrositlerden zengin kan hücreleri alanı, hemen üstünde lökositlerden zengin buffy coat olarak tanımlanan dar bir alan ve bunun üzerinde platelet ve serum alanı oluşmaktadır.
 Platelet ve serum bölümünde plateletler farklı konsantrasyonlarda bulunmakta. Serumun buffy coat yakın kısmında plateletler daha yoğun olduğu için bu alan plateletlereden zengin kısım-platelet rich plasma-PRP olarak tanımlanırken üstte kalan kısım plateletlerin daha az yoğun olduğu kısım-platelet poor plasma-PPP olarak tanımlanmakta.
Platelet ve serum bölümünde plateletler farklı konsantrasyonlarda bulunmakta. Serumun buffy coat yakın kısmında plateletler daha yoğun olduğu için bu alan plateletlereden zengin kısım-platelet rich plasma-PRP olarak tanımlanırken üstte kalan kısım plateletlerin daha az yoğun olduğu kısım-platelet poor plasma-PPP olarak tanımlanmakta.

3 lü musluk ve 5 ml lik luer lock enjektör ile platelet + serum kolayca 10 ml lik enjektörden alınabilir.
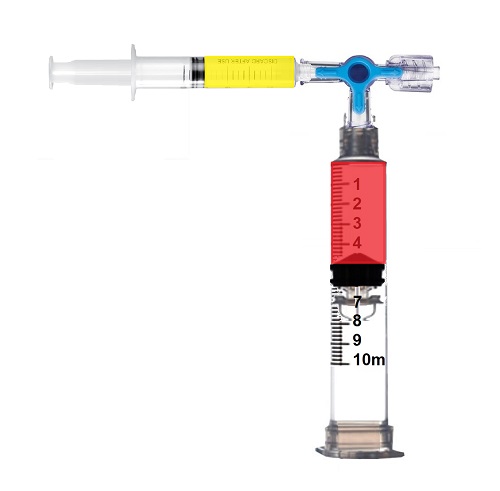
Yada 2 adet 5 ml luer lock enjektörlere PRP ve PPP ayrı ayrı alınabilir.
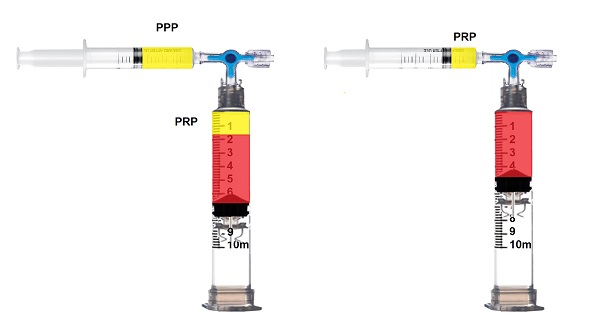
Platelet + serum bölümünde bilinmesi gereken bazı önemli bilgiler bulunmakta;
- Bunlardan ilki, bu karışımda ayrışan PRP ve PPP alanlarında platelet konsantrasyonlarının farklı olması ve bunun önemidir. Platelet konsantrasyonlarının normal kana göre 2.5, 3.5 ve 4.2–5.5 kat fazla olduğu serumlar ile fibroblast–osteoblast hücre kültürleri üzerinde çalışmalar yapılmıştır. Bu çalışmalarda hücre kültürlerinde hepsinde 72 saat sonra maksimum biyolojik aktivitenin başladığı görülmüştür. Ancak daha önemlisi, platelet konsantrasyonunun 2.5 kat fazla olduğu hücre kültürlerinde biyolojik aktivite daha fazladır. Platelet konsantrasyonu arttıkça hücrelerin çoğalması üzerindeki etkileri beklenenin tam tersi olmakta, yani baskılanmaktadır. Fibroblast hücrelerinde platelet ideal konsantrasyonunun başlangıç konsantrasyonunun 2-4 katı olması gerektiği gösterilmiştir. Bu nedenle PRGF jel kullanımı için PPP bölümü kullanılmaktadır.
- İkincisi, plateletlerin volümü. Platelet volümü ile platelet konsantrasyonu karıştırılmamalıdır. Plateletler, megakaryositik hücrelerin sitoplazmalarının parçalanması ile oluşan çekirdekleri olmayan hücrelerdir. Plateletler oluşurken megakaryositik sitoplazma eşit parçalanmadığı için kanda plateletlerin volümleri aynı değildir, yani değişkendir. Platelet sayısı ile her bir platelet volümü arasında negatif korelasyon bulunmaktadır (plateletler megakaryositlerden kaynaklandıklarına göre sayı ve volüm korele olmalıdır ki 1 megakaryositten kaynaklanan toplam platelet kütlesi sabit olsun). Büyük volümlü plateletler, daha fazla hücre membranı ve sitoplazmalarında daha fazla biyoaktif granül içermektedir. Granüllerin fazlalığı, büyüme faktörleri, enzimatik ve metabolik aktivitelerin daha fazla olmasına yol açmaktadır. Ayrıca aşağıda detaylı anlatılacak olan hücre membranından kaynaklanan ve serum proteinleri ile birlikte PRGF jel oluşumuna katılacak glikokaliks yapısının da fazla olması anlamına gelmektedir. Platelet sitoplazmasındaki granüllerde bazı büyüme faktörleri olduğunu biliyoruz. Bunlar: "platelet derived growth factor (PDGF), transforming growth factor-β1 (TGFβ1), epidermal growth factor (EGF), insulin-like growth factor-I (IGF-I), hepatocyte growth factor (HGF), basic fibroblast growth factor (bFGF) ve vascular endothelial growth factor (VEGF)" gibi. Bu nedenle son yıllarda PRP ve PRGF etkinliğinin değerlendirilmesinde platelet sayısı değil, ortalama platelet volümünden bahsedilmektedir.
-
Üçüncüsü, santrifüj hızı ve süresi. Yüksek santrifüjlerde öncesinde platelet aktivasyonu yapılmasa bile platelet membranlarının santrifüj sırasında yırtılması, büyüme faktörlerinin serbest kalmasını sağlamaktadır. Bu nedenle santrifüj hızları 580 g ya da 45 derecelik santrifüjlerde 100-1500 rpm ve 5 dakika olarak düzenlenmektedir. Düşük santrifüj hızları kullanılacaksa süre uzatılmalıdır.
PPP den PRGF jel elde edilmesi
1987 yılında kan plasması 80 derecede denatüre edilerek elektroforez yapıldığında yüksek moleküler ağırlıklı proteinler saptandı. İlk akla gelen bu moleküller içerisinde dolgularda kullanılan hyaluronik asit varlığı olabileceği ve bu proteinlerin deriye enjekte edildiğinde dolgu materyali olarak kullanılabileceği oldu. Yapılan çalışmalarda bu proteinlerin içerisinde hyaluronik asit oranlarının düşük olduğu gözlendi. Ancak 2020 yılında yapılan bir başka çalışmada PPP'nin 75 °C'de 10 dakika etüvlenmesi ile denatüre olan kan plasma proteinleri deriye enjekte edilmiş ve 21 gün dokuda kaldıkları gösterilmiştir. Bu, hyaluronik asit olmasa da kan plasma proteinlerinin dolgu olarak kullanım düşüncesini yeniden güçlendirmiştir. Bu arada kan plasması ve serumu gibi tanımları kullanırken bunları biraz açıklayalım.
Kan plazması, kan hücreleri olan eritrosit, lökosit ve trombositin içinde bulunduğu sıvı kısmıdır. Yukarıda anlatıldığı gibi alınan kana pıhtılaşmayı önleyen bir antikoagülan madde (sodyum sitrat gibi) eklenerek santrifüj edilirse altta kan hücreleri, üstte serum kalmakta, plazma değil. Sıklıkla kan serum ve plasmasını tanım olarak birbiri yerine kullanırız. Serumun plazmadan farkı, fibrinojen ve diğer bazı pıhtılaşma faktörlerini içermemesidir. Kan plazmasının %80-90’ını su ve %10-20'sini suda çözünmüş biyokimyasal maddeler oluşturur. Bu biyokimyasallar;
Kan plazmasındaki çözünmüş bu biyokimyasalların büyük çoğunluğunu proteinler oluşturmaktadır. Sağlıklı erişkin bir insanda kan plazma veya serumunun total protein düzeyi ortalama her 1 ml'de 57-80 mg kadardır ki bunun 35-50 mg kadarını serum albümin, 25-32 mg kadarını globülinler oluşturur. Plazmanın protein fraksiyonunda transaminazlar, dehidrojenazlar, peptidazlar, asit ve alkali fosfatazlar, aldolaz, α-amilaz, lipaz, katalaz, kolinesteraz, β-glukuronidaz gibi birtakım enzimler de bulunur.
Kan plazmasındaki azotlu maddeler; üre, amino asitler ve amino asit türevleri, ürik asit, kreatinin, kreatin, bilirubin gibi bileşiklerdir. Bunlar üre sağlıklı ve erişkin bir insanda 1 ml'de 2-4 mg, ürik asit 0.2-0.6 mg, kreatinin 0.05-0.1 mg, total bilirubin 0.001-0.1 mg, kan plazmasında çoğu glutamik asit olmak üzere total olarak 3.5-6.5 mg/dL düzeyinde serbest amino asit bulunur.
Kan plazmasında bulunan başlıca karbonhidrat glukozdur. Sağlıklı erişkin bir insanda 8-10 saatlik açlıktan sonra enzimatik yöntemlerle ölçülen 1 ml serumda glukoz düzeyi 6-10 mg/dL kadardır. 1 ml serumda 0.6-0.8 mg düzeyinde fruktoz, 0.5-0.6 mg düzeyinde glikojen, 0.2-0.4 mg düzeyinde pentozlar, 6-10.5 mg düzeyinde polisakkarit yapısına girmiş olarak glukozamin de bulunur.
Kan plazmasında sitrik asit, α-ketoglutarik asit, malik asit, süksinik asit, asetoasetik asit, pirüvik asit, laktik asit gibi organik asitler de bulunur.
Kan plazmasında bulunan lipidler; trigliseridler, yağ asitleri, fosfolipidler, kolesterol ve kolesterol esterleridir; lipidlerin büyük kısmı β-lipoprotein (LDL, düşük dansiteli lipoprotein) halinde bulunur. 1 ml kan plazması veya serumunun total lipid düzeyi ortalama olarak sağlıklı ve erişkin bir insanda 61.7 mg, total kolesterol düzeyi 18.1 mg, trigliserid düzeyi 5-15 mg, total fosfolipid düzeyi 15-25 mg kadardır ki serumda en fazla bulunan fosfolipid lesitindir. 1 ml serumda total yağ asidi düzeyi 15-50 mg ve serbest yani esterleşmemiş yağ asidi (FFA) düzeyi 0.8-3 mg kadardır.
Kan plazmasında bulunan inorganik bileşikler, katyonlar ve anyonlar halindedirler. 1 lt serumda total olarak 142-155 mEq düzeyinde olan katyonların en bol bulunanları Na+ ve K+, total 142-155 mEq/L düzeyinde olan anyonların en bol bulunanları klorür ve bikarbonattır.
Santrafüj sonrası elde edilen serumda zengin kan plazma proteinleri, plateletler ve bunlara ait biyoaktif maddeler bulunmakta ve PRGF jeli bundan elde ediyoruz. Peki, hangi kısımdan?
Sodyum sitrat eklenmiş venöz kanın santrifüjü sırasında elde edilen serumun en üst bölümünde küçük sitoplazmalı trombositler, ortada orta sitoplazmalı trombosit ve az miktarda lökosit; en altta, buffy coat'ın üstünde ise büyük sitoplazmalı trombositler ve daha yoğun lökositler bulunmakta. Serumun en üst 1/3'ünde %6, orta 1/3'ünde %14 ve alt 1/3'ünde %28 trombosit bulunmakta. Serumun en üst 1/3'ünde trombosit konsantrasyonu en düşük ve trombositler küçük sitoplazmalı. Bu alanda serum plazma proteinleri daha fazla anlamına gelmekte (ne kadar fazla plazma proteini, o kadar fazla PRGF jel). Büyük sitoplazmalı trombositler ve lökositler içeriklerinde daha fazla DNA ve RNA içermekte. Bunlar plazma proteinleri gibi ısı ile denatüre olmamakta ve jel formuna katılmamakta. Ayrıca lökositler ısıya dirençli olmak dışında sitokin üretimleri ile dokuya enjekte edildiğinde daha fazla inflamasyona neden olmakta. Hatta lökosit içeriğinde nötrofiller var ise, bunlar enjekte edildiğinde doku hasarına bile neden olabilmekte (nötrofiller seçici olmayan toksik serbest oksijen yapmakta; hipoklorit, süperoksid ve hidroksil radikalleri gibi). Fibroblastlar hücre kültürlerinde platelet ideal konsantrasyonunun başlangıç konsantrasyonunun 2-4 katı olması gerektiğini yukarıda bahsetmiştik.
Bu bilgilerden sonra jeli hazırlamaya devam edelim. Sodyum sitrat eklenmiş venöz kanın santrifüjü sonrasında elde edilen serumun 1/2 en üst bölümü alınarak kalsiyum (kalsiyum glukonat, kalsiyum levulinat) eklenmekte. Kalsiyum, trombositlerin şişerek hücre membranlarının yırtılmasına neden olmakta. Bu, platelet içerisindeki granüllerdeki büyüme faktörleri gibi aktivatörlerin serbest kalması anlamına gelmekte. Bu süreç düşük ısılarda daha iyi gerçekleşmekte. Kalsiyum eklenmesi ve düşük ısılarda bekletilmesi serumdaki küçük çaplı proteinler ve glikokaliksi (glycocalyx) aktive etmekte. Glikokaliks, hücre membranı yüzeyinde bulunan karbonhidrat yapısında ve kan plasmasıyla platelet sitoplazması arasında yarı geçirgen bir bariyer oluşturmakta. Glikokaliks, platelet membranı yüzeyinde hyaluronik asit, kondroitin ve heparin sülfat ile birlikte bir kompleks yapı oluşturmakta. Platelet dışındaki glikokaliks yapısının diğer kan hücrelerine göre daha kalın olduğu gösterilmiştir.
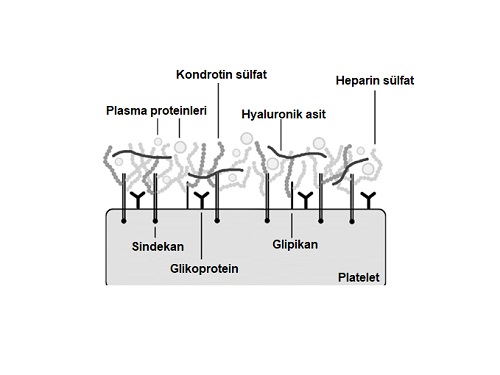
Serumun 1/3 en üst bölümü, PPP alınarak her 2.2 ml sine 0.1 ml % 10 luk kalsiyum(kalsiyum glukonat, kalsiyum levulinat) eklenmekte. Kalsiyum eklendikten sonra 0 °C de 10 dakika bekletilmekte.

Plasma proteinleri ve glikokaliks'ten oluşan bu kompleks, serum içerisine vitamin C eklenerek etüvde 50 °C üzerinde ısıtılmakta. Tüm kompleks yapı jel formuna dönmekte ve vitamin C, jeldeki proteinlerin stabilitesini sağlamaktadır. Vit. C, bu stabilite dışında enjekte edildiği dokuda yeni kolajen yapımını uyarmakta, dokuda antioksidan etkisi ile inflamasyonu ve oksidanların doku hasarını engellemektedir. Komple serumun her 1 ml'sine 0.3 ml vitamin C eklenerek 70-85 °C'de etüve alınmaktadır.
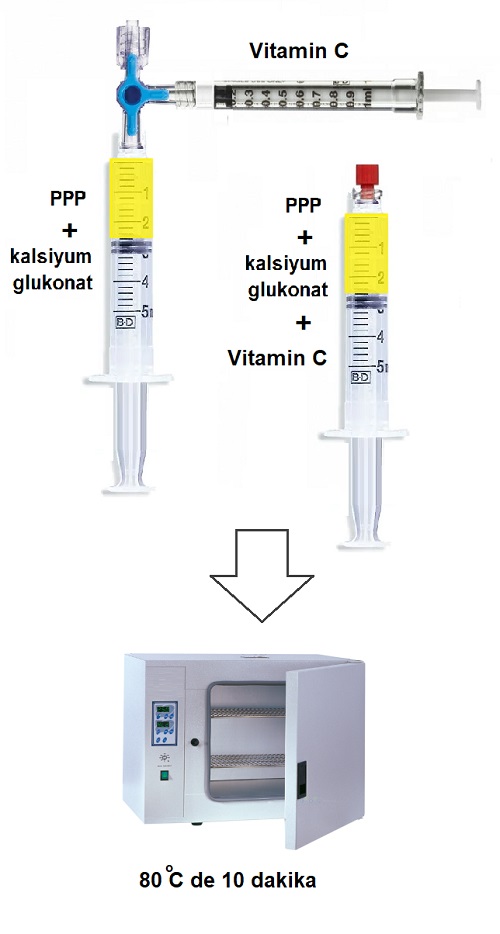
Etüvde bekleme süresi, elde edilen jelin viskozitesini değiştirmekte. Örneğin, 76 °C'de 12 dakika bekletildiğinde yüksek viskozitede jel (HVG) elde edilirken, aynı ısıda 8 dakika bekletildiğinde düşük viskozitede jel (LVG) elde edilmektedir. Bu farklı viskoziteler, daha sonra anlatacağımız doku jelinin deride derin ve yüzeysel kullanımı için önemlidir. Etüv sonrası yarı saydam sarımsı serum kompleksinden sarımsı ve opak jel elde edilmektedir. Aşağıda, üst solda görüldüğü gibi, jel 25 g iğneden çıktığında bile 3 boyutlu formunu koruyacak kadar viskoelastik ve pseudoplastik özellikte.
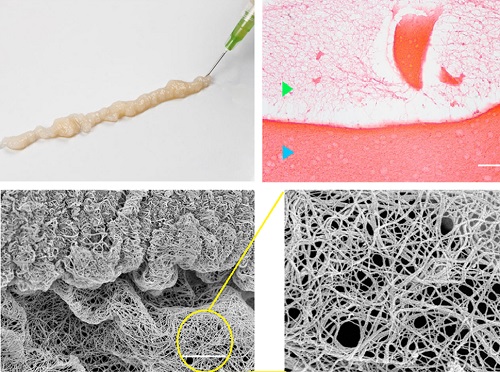
Bu jel hemotoksilen eosin ile boyanarak ışık mikroskobunda bakıldığında; yukarıda üst sağ resimde mavi okla gösterilen alanda jelin yoğun, yeşil okla gösterilen alanda daha az yoğun fibrin ağlarından oluştuğu görülmektedir. Serumda bulunan yüksek moleküler ağırlıklı proteinler ve glikokaliksler denatüre olarak kararlı bir fibrin ağı oluşturmakta. Bu fibrin yukarıda alt sağ ve sol resimlerde elektron mikroskopta görüntülenmiştir. Kararlı fibrin ağ yapısının arasındaki boşluklar, doku jeli deriye enjekte edildiğinde, adhezyonla deri hücrelerinin (fibroblastlar gibi) gelip bu boşluklara yerleşip büyüyebileceği uygun bir ortam oluşturmaktadır.
Bu jelin hidrasyon oranı % 91 ± 1 ve jelin hazırlanması sırasında plasmayı oluşturan su tarafından yeteri kadar hidrate olmaktadır. Doku jeli enjekte edildiğinde ilk 72 saat içerisinde dokuda suyu bağlamakta ancak hidrate olduğu için ancak enjekte edildiği volümün % 15'i kadar su tutmaktadır. Bu da uygulama alanında daha hafif bir ödem gelişebilmesi anlamına gelmektedir.
Başlangıçta elde edilen serumun 1/3 en alt bölümü yani PRP alınarak her 2.2 ml'sine 0.1 ml % 10'luk kalsiyum (kalsiyum glukonat, kalsiyum levulinat) eklenmektedir. Kalsiyum eklendikten sonra 0 °C'de 10 dakika bekletilmektedir. Plateletlerin yoğun olduğu serumun bu alanından böylece daha fazla platelet kaynaklı büyüme faktörleri gibi biyolojik aktif maddeler elde edilmektedir. PRP direkt hastaya klasik yüz PRP uygulaması şeklinde uygulanabileceği gibi sıklıkla 5:1 oranında jel ile karıştırılarak uygulanabilmektedir.
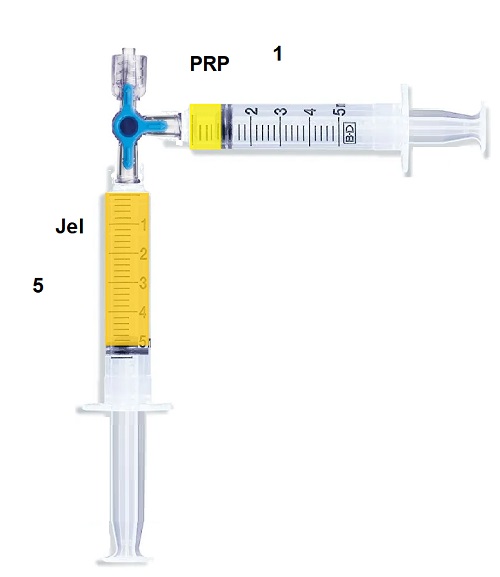
Bu karışım içeriğinde platelet kaynaklı zengin biyolojik aktif maddeler ve jel formunda denatüre plazma proteinleri bulunduğu için "platelet rich growth factors gel - PRGF jel" olarak tanımlanmaktadır.
PRGF jel, kozmetik amaçlı kullanılan dolgulara göre birçok avantaj sunmaktadır:
- Hastanın kanından elde edilmesi, otolog yüksek bir biyolojik uyum sağlamaktadır.
- 3 boyutlu fibrin yapısı ve ara boşlukları ile enjekte edildiği dokuda hücrelerin bu yapı içerisinde çoğalabilmelerini sağlamaktadır.
- Platelet kaynaklı biyolojik aktif maddeler içermesi, doku onarımı ve yenilenmesini sağlamaktadır.
Aseptik ve kontaminasyonun engellendiği koşullarda PRGF jelinin hazırlanarak taze uygulanması, diğer dolgu ürünlerinin birçok olumsuzluğuna göre (diğer dolguların üretimi, ambalajlanması, dağıtımı, ofis saklanma koşulları, dolgu marka seçimi, FDA, CE ve T.C. Sağlık Bakanlığı izni olup olmaması, yüksek maliyetleri...) üstünlükler sağlamaktadır.
Doku jelinin hazırlanması sırasında yukarıda anlatıldığı gibi jele farklı vizkoziteler (yüksek-HVG ve düşük-LVG) kazandırılabilmektedir. Bu jelin deride yüzeysel olarak kırışıklıklar altına (intradermal) ya da deride derin volüm verme amaçlı (subdermal) uygulanmasını sağlamaktadır.
PRGF jelinin vizkoelastik yapısı reolojik çalışmalar ile kontrol edildiğinde 18-30 G iğneler ya da kanüller ile uygulanabilirliği gösterilmiştir.
HVG ve LVG ile yapılan deride yüzeysel ve derin enjeksiyon sonrası ultrason (US) ile değerlendirmede enjeksiyon derinliklerinde PRGF jelinin stabil durduğu görülmektedir.
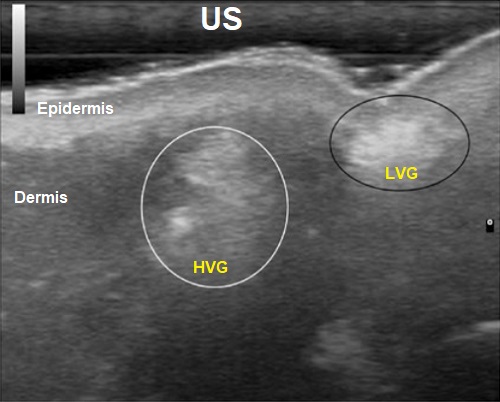
PRGF jel hazırlanmasında platelet sayımları yapılmış ve 2.1 X ± 0.7 değerleri elde edilmiştir. Bu plateletlerin istenen hedef değerine çok yakın olduğu görülmektedir. Her iki jelde, yani HVG ve LVG'de biyoaktif proteinlere bakıldığında, değerleri istenilen düzeydedir. Aşağıdaki tabloda bunlar özetlenmiştir.
HVG ve LVG yapılan reolojik değerlendirmeler, vizkoelastik ve pseudoplastik özelliklerinin enjekte edilebilir dolgu amacıyla kullanılabileceğini göstermektedir. HVG, deride derin uygulamalar ile volüm eksikliklerini karşılarken, LVG yüzeysel volüm uygulamaları için uygundur. Aşağıdaki tabloda bunlar özetlenmiştir.
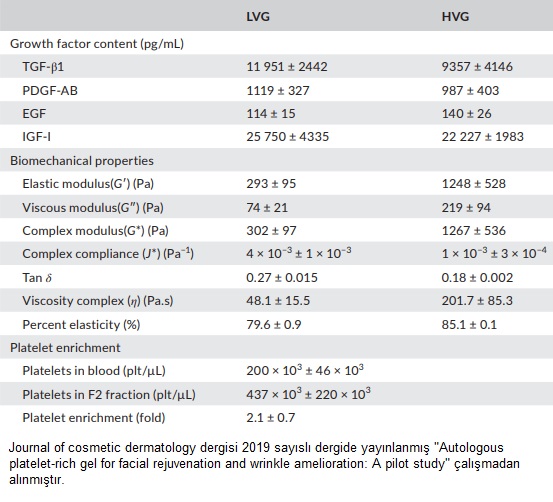
HGV ve LVG jellerin kültür ortamında yapılan doku plasminojen aktivatörlerine maruz bırakıldığında 14. günde başlangıç volümlerinde azalma oranları sırasıyla %13 ± 2 ve %14 ± 6 olarak bulunmuştur. 4-6 ay dokuda klinik etkinlikleri devam etmektedir.
Her iki jelin uygulandığı doku kültürlerinde 72 saat sonunda fibroblast hücre çoğalmasında 1.45 ve 1.55 kat artış gözlenmiştir.
PRGF jel, kadınlarda gebelik ve süt emzirme sırasında, uygulama alanında enfeksiyon ve inflamasyon durumlarında, onkolojik öykülerde, romatizma gibi konnektif doku hastalıklarında, antikoagülan ve immünosüpresif ilaç kullanımında, yüzde uygulama alanında implant bulunmasında, kan ürünlerine karşı alerjik reaksiyonları olanlarda kullanılmamaktadır.

